Štruktúra butanónu, vlastnosti a použitia
- 4318
- 603
- Valentín Dula
Ten Vylučovať Je to organická zlúčenina, konkrétne ketón, ktorého chemický vzorec je Cho3Chvály2Cocha3. Jeho vzhľad je vzhľad bezfarebnej kvapaliny, ktorá sa v zásade používa ako rozpúšťadlo. Má podobné vlastnostiam acetónu, ale varte pri vyššej teplote a pomalšie sa odparuje.
Vytvára sa katalytickou dehydrogenáciou 2-butanolu (chirálna zlúčenina). Je však v prirodzenom stave v zložení niektorých ovocia. Je súčasťou emanácií výfukových potrubí vozidiel a je súčasťou dymu tabaku.
 Butanón. Zdroj: Pixabay.
Butanón. Zdroj: Pixabay. Je to po acetóne najjednoduchšie z tejto rodiny organických zlúčenín. Butnonón spôsobuje podráždenie v očiach a nose. V nezvyčajne vysokej dávke môže spôsobiť podráždenie pľúcnej sliznice. Na druhej strane sa táto kvapalina považuje za predchodcu narkotík.
Butanone má veľkú rozpustnosť vo vode; Ale je tiež veľmi rozpustný v organických rozpúšťadlách, ako je etanol, éter, acetón, benzén a chloroformy. Dalo by sa to vysvetliť, pretože jeho hodnota P log (0,29) pre koeficient priečok oktánu/voda je nízka.
[TOC]
Butanónová štruktúra
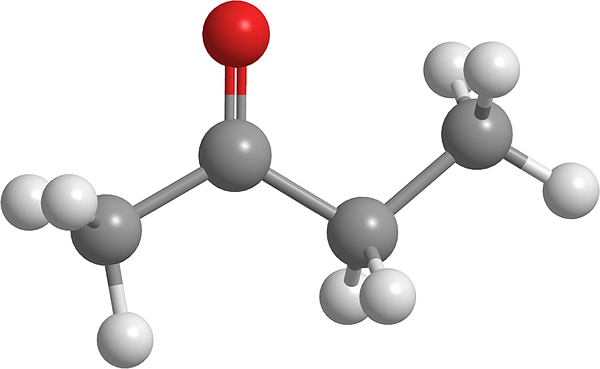
Na hornom obrázku je molekula butanónu znázornená s guľovými a stĺpcovými modelmi. Atóm kyslíka skupiny karbonylovej skupiny (červená guľa) je možné vidieť v druhom uhlíku. Táto skupina, C = o, je zodpovedná za udelenie trvalého dipólového momentu molekule.
Butanone, štrukturálne pohľad, nie je nič viac ako acetón, ku ktorému bola pridaná metylénová skupina, ch2. Moment, ktorý má viac uhlíkov, je dipólový moment menší v porovnaní s acetónom; Ale jeho najväčšia molekulárna hmota spôsobuje, že sa vari pri vyššej teplote.
Táto molekula, rovnako ako iné ketóny, nemá možnosť formovania vodíkových mostov; A preto ich interakcie dipólu-dipolo nie sú také silné.
Môže vám slúžiť: emulgátor: proces emulzie, molekulárne aspekty, aplikáciePreto je to prchavá kvapalina. Keď teplota klesne (-86,6 ° C), jej slabé dipóly sú tie, ktoré vedú svoje molekuly, aby vytvorili kryštál. Okrem toho možno tiež poznamenať, že butanón je štrukturálne asymetrický.
Vlastnosti
Molekulárna receptúra
C4H8Alebo CH3Cocha2Chvály3
Mená
- Vylučovať.
- 2-butanón.
- Butan -2 -ona.
- Metyl ethil Cetona.
Molárna hmota
72,107 g/mol.
Fyzický popis
Bezfarebná tekutina.
Vôňa
Voňavý na mincovňu, mierne silný.
Bod varu
79,59 ° C pri 760 mmHg.
Bod topenia
-86.6 ° C.
zapaľovač
-9 ° C (zatvorený šálka).
Rozpustnosť
29 g /100 ml pri 20 ° C. Zatiaľ čo jeho dipólový moment je menší ako moment acetónu, môže stále vo vynikajúcej miere interagovať s molekulami vody. Z nich prijíma mosty vodíka: (Chy3) (Ch2Chvály3) C = o-hah. Z tohto dôvodu je vo vode veľmi rozpustné.
Rozpustnosť v organických rozpúšťadlách
Rozpustný v benzéne, alkoholu a éteru; Misilné s olejmi, etanolom, éterom, acetónom, benzénom a chloroformom. Všimnite si, že butanón je rozpustný v rôznych rozpúšťadlách.
Hustota
0,7997 g/cm3 pri 25 ° C.
Hustota
2,41 (vo vzťahu k vode = 1).
Tlak vodnej pary
90,6 mmHg pri 25 ° C.
Koeficient priečneho októbra/vody
Log p = 0,29
Teplota
505 ° C.
Rozklad
Rozkladá sa fotochemickými procesmi oxidáciou bezplatným hydroxyl radikálom. Keď sa zahrieva na rozklad, vydáva akerový dym.
Hrebeň
0,40 CPoise pri 25 ° C.
Spaľovacie teplo
2.444,1 kJ/mol pri 25 ° C.
Odparovanie
31,30 kJ/mol v bode varu; a 34,79 kJ/mol pri 25 ° C.
Môže vám slúžiť: Všeobecný plynový zákonPovrchové napätie
23,97 Mn/m A 25 ° C.
Ionizačný potenciál
0,54 eV.
Prah
Nízka vôňa: 0,735 mg/m3.
Vysoký zápach: 147,5 mg/m3.
Index lomu
1 788 až 20 ° C.
Disociačná konštanta
Pka = 14,70.
Stabilita
Stabilný, ale veľmi horľavý. Nezlučiteľné s oxidačnými činidlami, základňami a silnými redukčnými činidlami. Malo by sa vyhnúť vlhkosti.
Žiadosti
Solventný
Butanone sa používa ako rozpúšťadlo pri vypracovaní povrchových povlakov, výroby bezdymového prachu, vypracovania farebných živíc a pri odstraňovaní akumulácie tuku produkovaných mazivami.
Okrem toho sa používa pri vypracovaní:
- Umelá koža.
- Gomasy.
- Lakas.
- Lak.
- Lepidlo.
- Rozpúšťadlo.
- Náter.
- Lepky.
- Plastové cementy.
- Tmel.
- Magnetické pásky.
- Priehľadný papier.
- Tlačiť.
- Kozmetika a farmaceutické výrobky.
Používa sa tiež ako rozpúšťadlo na vymedzenie kovových povrchov, čistiacich prostriedkov na elektronické vybavenie a extrakciu tukov. Slúži na ťažbu tvrdého dreva a rastlinný olej.
Je to inertná zložka pri vypracovaní pesticídov a pri výrobe dusičnanu acetátu a celulózy.
Používa sa ako extrakčný rozpúšťadlo pri spracovaní potravín a zložiek potravín; Napríklad pri frakcionácii tukov a olejov, ako aj v procese deakfeinácie kávy. Používa sa tiež ako rozpúšťadlo v markeroch používaných v bielych doskách.
Činidlo
- Butanone sa používa ako vo vode rozpustný fotoiniciátor.
- Kondenzuje s formaldehydom na výrobu ketónu izopropenilu.
- Zažiť autokodenzáciu na výrobu etyl amylo cetona.
- Reaguje s citralou, aby sa získalo zložky parfumov, ako je metylpseudoionón.
Môže vám slúžiť: reakčné teplo- Zasahuje ako katalyzátor pri výrobe hydrakcínu.
- Okrem toho je prekurzorom peroxidu metyletyl -cetony, ktorý je katalyzátorom niektorých polymerizačných reakcií.
Plastový cement
Butanone má aplikáciu ako plastové zváracie činidlo s použitím pri zostavovaní modelov polystyrénovej mierky. Butnonón rozpustí polystyrén, čo umožňuje, aby sa okraje spojili, keď dôjde k novej polymerizácii. Toto správanie je cementu a nie lepidla.
Iné použitia
Butanone sa používa ako sterilizátor spór baktérií v chirurgických nástrojoch, ihloch, podkožných injektoroch a zubných nástrojoch.
Používa sa ako ochucovacie činidlo potravín vo veľmi nízkych koncentráciách; Napríklad v alkoholických nápojoch je koncentrácia 20 ppm; v pečených výrobkoch, 12,7 ppm; Mäso má asi 26,5 ppm; žuvacia guma, 0,63 ppm; a v tukoch a olejoch, 1,0 ppm.
A nakoniec, butanón sa používa pri separácii hemoproteínovej skupiny apoproteínu v hemoproteínoch.
Odkazy
- Morrison, r. Tón. a Boyd, R, N. (1987). Organická chémia. 5ubytovať sa Vydanie. Redakčný Addison-Wesley Inter-American.
- Carey F. (2008). Organická chémia. (Šieste vydanie). MC Graw Hill.
- Graham Solomons t.W., Craig B. Fryhle. (2011). Organická chémia. Amín. (10thVydanie.). Wiley Plus.
- Národné centrum pre biotechnologické informácie. (2019). Databáza pubchem metyletytón. CID = 6569. Získané z: pubchem.Ncbi.NLM.NIH.Vláda
- Wikipedia. (2019). Vylučovať. Zdroj: In.Wikipedia.orgán
- Kráľovská spoločnosť chémie. (2015). Vylučovať. Chempider. Obnovený z: ChemSpider.com
- Arlem Cheprasov. (2019). Čo je butanone? Vzorec a použite. Štúdium. Získané z: štúdie.com
- Ben Verve. (17. mája 2017). Vylučovať. Svet chémie. Získané z: Chemistryworld.com

