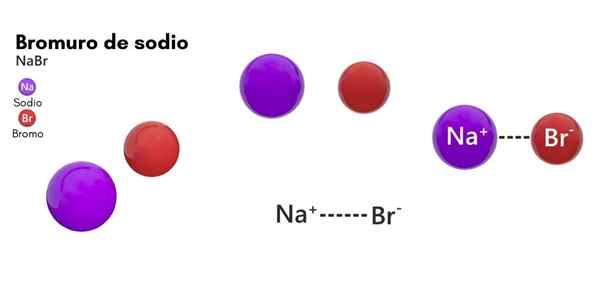
Bromid sodný (NABR)
- 4496
- 870
- Tomáš Mydlo
Čo je bromid sodný?
On bromid sodný Je to chemický druh, ktorý patrí do soli anorganického pôvodu. Jeho štruktúra sa skladá z bromického halogénu a kovového prvku sodného v 1: 1. Jeho chemický vzorec je NABAB a je v stave pevnej agregácie v štandardných teplotných podmienkach (25 ° C a 1 atm).
Normálne sa dá pozorovať ako biely prach a považuje sa za zlúčeninu kryštalického typu, ktorá tiež vykazuje hygroskopické správanie; to znamená, že má schopnosť absorbovať vlhkosť zo svojho okolia.
Podobne má bromid sodný fyzikálne vlastnosti veľmi podobný inej iónovej zlúčenine toho istého kovu: chlorid sodný. Tento chlorid je znázornený ako NaCl, ktorý je častejšie známy ako bežná soľ alebo stolová soľ.
Má veľké množstvo použití v rôznych oblastiach vedy; Napríklad sa používa pri výrobe rôznych typov liekov (sedatíva, hypnotiká, antikonvulzívne, okrem iného), ako v organickej syntéze a dokonca aj vo fotografických aplikáciách.
Chemická štruktúra
Bromid sodný je prezentovaný v tuhej fáze a rovnako ako mnoho iných solí anorganickej povahy, má kryštalickú štrukturálnu konformáciu.
Táto kryštalická molekula, vytvorená brómom a jedným z vodíka, má kubickú konformáciu zameranú na tváre, ako sú haloidové soli toho istého kovu (NAI, NAF a NaCl).
Toto molekulárne usporiadanie tvorí štrukturálny základ mnohých zlúčenín, v ktorých sa poradie vykonáva tak, aby sa každý ión udržiaval v strede oktaedrického obrázku, ako je znázornené na nasledujúcom obrázku.
Môže vám slúžiť: kyselina fosfor (H3PO3)
V tomto type skla môžete vidieť, ako má každý z iónov okolo neho ďalších šesť iónov - ktoré majú protichodný elektrický náboj - ktoré sa nachádzajú na koncoch oktaedrickej postavy.
Podobne aj štruktúra tejto iónovej látky naznačuje, že má vysoký bod topenia približne 747 ° C, ktorý je komerčne vo svojich dvoch formách: bezvodý druh (bez molekúl vody) a dihydratovaný druh (s dvoma molekulami vody v jej štruktúrnom vzorec (NABR · 2H2O)), ktorých body zlúčenia sú rôzne.
Chemická syntéza
Bromid sodný pochádza z chemickej reakcie, ktorá sa vyskytuje medzi vodíkovým bromidom (BRH, halogenidom vodíka v plynnej fáze) a hydroxidom sodným (NaOH, silnou bázou v tuhej fáze a hygroskopickými vlastnosťami).
Týmto spôsobom sa vyrába komerčne a pridáva prebytok brómu do roztoku NaOH. Teda sa vytvorí zmes brromidu/brómu. Následne sú výsledné produkty podrobené odparovaniu, kým nie sú suché, a sú ošetrené uhlíkom, aby sa vytvorila reakcia bromátového iónu (bro3-) do bromidového iónu (br-).
Neutralizácia
Podobne sa táto anorganická soľ môže vyskytnúť aj prostredníctvom neutralizačnej reakcie uhličitanu sodného (NA2Co3) S kyselinou bromovou (Hbro3), podľa rovnakého postupu opísaného vyššie.
Prostredníctvom syntézy sa táto látka môže produkovať reakciou medzi železom s brómom a vodou. Ako produkt tejto reakcie pochádza druh ferózne -ferického bromidu.
Môže vám slúžiť: alkoholyNásledne sa tento druh vytvoril (reprezentovaný ako február2/Február3) sa rozpustí vo vode a pridáva sa určité množstvo uhličitanu sodného. Nakoniec sa roztok filtruje a prechádza procesom odparovania, aby sa konečne získal bromid sodný.
Vlastnosti bromidu sodného
- Je bežne v stave pevnej agregácie, vo forme bieleho prachu.
- Má kryštalickú štruktúru s molekulárnym poradím vo forme kocky vycentrovanej na tvári.
- Bod topenia tejto látky je približne 747 ° C pre bezvodý a tvar 36 ° C pre jeho dihydrátovú formu, ktorá predstavuje rozklad skôr, ako sa topí.
- Je tvorený sodíkovým iónom (NA+) a bromidový ión (br-) s molárnou hmotnosťou alebo molekulovou hmotnosťou 102,89 g/mol.
- Jeho bod varu je pomerne vysoký a pozoruje 1390 ° C (ekvivalent k 2530 ° F alebo 1660 K).
- Rozpustnosť tohto druhu je okolo 94,32 g/100 ml vo vode pri 25 ° C, čo sa zvyšuje, keď sa teplota zvýši.
- Tým, že sa podstúpi zahrievanie do bodu, keď sa rozpadá, táto látka uvoľňuje brómové plyny a oxid sodný považovaný za toxický.
- Hustota bezvodej formy bromidu sodného je 3,21 g/cm3, Zatiaľ čo dihydratovaná zlúčenina je 2,18 g/cm3.
- Jej rozpustnosť v alkoholu sa považuje za miernu, ako v iných rozpúšťadlách, ako je pyridín, amoniak a hydrakcia.
- Predstavuje nerozpustnosť proti acetonitrilu a acetone.
Použitie/aplikácie
- V lekárskej oblasti sa používa ako liek pre veľké množstvo stavov, ktoré pochádzajú za záchvaty a ako terapia, aby sa zabránilo obrázkom epilepsie u pacientov so syndrómom Wolf-Hirschhorn, ako aj u sedatívnej a hypnotickej liečby.
Môže vám slúžiť: Kyselina bromová (HBRO3): Vlastnosti, riziká a použitia- Vo veterinárnej medicíne sa používa u psov, ktoré majú kŕčovne poruchy v dôsledku vedľajších účinkov liekov, ako je primidón alebo fenobarbitál.
- V oblasti ropného priemyslu sa používa v procesoch prípravy určitých tekutín rôznorodej hustoty, ktoré sa používajú v ropných vrtoch.
- V oblasti biologického výskumu sa preukázali jeho mikrobiokidné vlastnosti; to znamená, že sa používa na kontrolu vývoja rôznych typov baktérií.
- V určitej syntéze organického typu sa táto anorganická soľ používa na prípravu iných druhov, ktoré predstavuje Bromo. Napríklad podľa Finkelsteinovej reakcie sa získavajú určité reaktivity alkyl halogenidy, z ktorých jeden sa vo fotografii používal celkom používaný.
- V oblasti čistenia a dezinfekcie sa bromid sodný používa v kombinácii s chlórom na hygienu veľkých objemov vody, ako v bazénoch a vírivke.