Štruktúra čerpadla sodného draselného, funkcia, mechanizmus, dôležitosť
- 3770
- 1125
- MUDr. Miloslav Habšuda
Ten Bomba sodného draslíka Je to proteínová štruktúra zahrnutá do širšej sady molekúl prítomných v mnohých bunkových membránach a ktoré sú zodpovedné za aktívny transport iónov alebo iných malých molekúl proti jeho koncentračným gradientom. Používajú energiu uvoľňovanú hydrolýzou ATP, a preto sa všeobecne nazývajú Atasas.
Čerpadlo sodíka draselného je AtPay Na+/K+, pretože uvoľňuje energiu obsiahnutú v molekule ATP na pohyb sodíka vo vnútri bunky a zároveň zavádza draslík draslík.
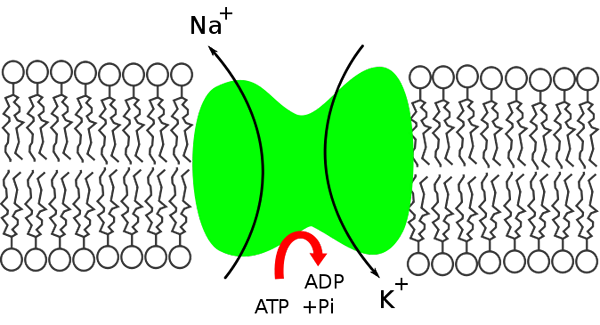
 Schéma bomby sodného draselného. Exteriér a interiér bunky. (Zdroj: Miguelferig, Via Wikimedia Commons)
Schéma bomby sodného draselného. Exteriér a interiér bunky. (Zdroj: Miguelferig, Via Wikimedia Commons) Vo vnútri bunky je sodík menej koncentrovaný (12 mEq/l) ako vonku (142 meq/l), zatiaľ čo draslík je koncentrovanejší vonku (4 mEq/l) ako vo vnútri (140 mEq/l).
Bomby Atasas sú klasifikované do troch veľkých skupín:
- Iónové čerpadlá typu F a V: Sú to dosť zložité štruktúry, môžu sa skladať z 3 rôznych typov podjednotiek transmarketov a až 5 pridružených polypeptidov v cytosóle. Fungujú ako protónové transportéry.
- ABC superrodina (angličtiny DoTp-BUviesť CUdelenie = ATP Union Cassette): integrované viac ako 100 proteínmi, ktoré môžu fungovať ako iónové dopravníky, monosacharidy, polysacharidy, polypeptidy a dokonca aj iné proteíny.
- Iónové čerpadlá triedy P: Tvorované aspoň jednou transmembraálnou alfa katalytickou podjednotkou, ktorá má miesto únie pre ATP a menšiu β podjednotku. Počas transportného procesu je a podjednotka fosforyila, a teda jej názov „P“.
Bomba draselného sodíka (Na+/K+ATPASA) patrí do skupiny iónových čerpadiel triedy P a objavil ju v roku 1957 Jens Skou, dánsky výskumný pracovník, keď študoval mechanizmus pôsobenia anestetík v nervoch krabov (Karcinus); Práca, za ktorú bola udelená Nobelova cena v chémii v roku 1997.
 Bomba sodného draslíka. Nakpompe2.JPG: Phi-Gastrein pri studene.WikipediaDerivatívne dielo: Sonia/CC By-S (http: // creativeCommons.Org/licencie/By-SA/3.0/)
Bomba sodného draslíka. Nakpompe2.JPG: Phi-Gastrein pri studene.WikipediaDerivatívne dielo: Sonia/CC By-S (http: // creativeCommons.Org/licencie/By-SA/3.0/) [TOC]
Štruktúra čerpadla sodného draselného
Čerpadlo sodíka draselného je enzým, ktorý z hľadiska kvartérnej štruktúry tvorí 2 proteínové podjednotky ALFA (a) a dva beta typy (β).
Je to preto tetramér typu a2p2, ktorého podjednotky sú komplexné membránové proteíny, to znamená, že prechádzajú lipidovou dvojvrstvou a majú intra aj extra cytosolické domény.
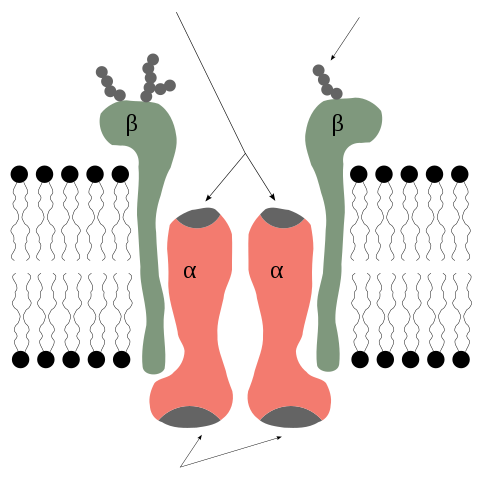 Alpha a beta podjednotky draslíka čerpadla. Rob Cowie/CC BY-SA (http: // creativeCommons.Org/licencie/By-SA/3.0/)
Alpha a beta podjednotky draslíka čerpadla. Rob Cowie/CC BY-SA (http: // creativeCommons.Org/licencie/By-SA/3.0/) Podjednotky
A podjednotky sú tie, ktoré obsahujú miesta Únie pre ATP a pre ióny Na+ a K+ a predstavujú katalytickú zložku enzýmu a tou, ktorá uplatňuje funkciu samotnej bomby samotnej bomby.
A podjednotky sú polypeptidy s veľkou veľkosťou s molekulovou hmotnosťou 120 kDa, 10 transmembranálnych segmentov a ich koncami N-a C-koncov umiestnených na cytosolickej strane.
Majú na intracelulárnych vedľajších miestach odborov pre ATP a pre Na+, ako aj zvyšok aspartátu v polohe 376, ktorý predstavuje miesto utrpené fosforylačným procesom počas aktivácie pumpy.
Väzbové miesto pre K+ je zjavne na extracelulárnej strane.
Beta podjednotky
Nezdá sa, že by β podjednotky nemajú priamu účasť na funkcii čerpania, ale v ich neprítomnosti sa uvedená funkcia nevyskytuje.
Publiky β majú molekulovú hmotnosť asi 55 kDa a sú glykoproteínymi s jednou transmarketovou doménou, ktorej glucidový odpad je vložený do extracelulárnej oblasti.
Môže vám slúžiť: bazálny list: Charakteristiky, histológia a funkcieZdá sa, že sú potrebné v endoplazmatickom retikule, kde by prispeli k správnemu skladaniu a podjednotiek a a potom na úrovni membrány na stabilizáciu komplexu.
Oba typy podjednotiek sú heterogénne a boli doteraz opísané izoformy a1, a2 a a3 pre UNA a p1, β2 a p3 pre ostatné. A1 sa nachádza v membránach väčšiny buniek, zatiaľ čo a2 je prítomný vo svaloch, srdci, tukovom tkanive a mozgu a a3 v srdci a mozgu.
Izoforma β1 je najviac šírivá distribúcia, hoci v niektorých tkanivách, ako sú vestibulárne bunky vnútorného ucha a glykolytické svalové bunky, chýba, hoci chýba. Ten obsahuje iba β2.
Rôzne štruktúry podjednotiek, ktoré tvoria čerpadlo Na+/K+ v rôznych tkanivách.
Funkcia draslíka
Plazmatická membrána predstavuje v prípade kedykoľvek zvážená plazma.
Obidve kompartmenty majú zloženie, ktoré sa môžu kvalitatívne líšiť, pretože vo vnútri buniek sú látky, ktoré nie sú mimo nich a extracelulárna tekutina obsahuje látky, ktoré nie sú prítomné intracelulárne.
Látky, ktoré sú prítomné v oboch kompartmentoch, sa dajú nájsť v rôznych koncentráciách a tieto rozdiely môžu mať fyziologický význam. To je prípad mnohých iónov.
Údržba homeostázy
Čerpadlo Na+/K+ plní základnú funkciu pri udržiavaní intracelulárnej homeostázy kontrolou koncentrácií iónov sodíka a draselných iónov. Táto údržba homeostázy to dosiahne vďaka:
- Iónová preprava: Predstavuje sodné ióny a vylučuje ióny draslíka, proces, ktorým tiež podporuje pohyb iných molekúl cez iné transportéry, ktoré závisia buď od elektrického náboja, alebo od vnútornej koncentrácie týchto iónov.
- Ovládanie objemu buniek: Úvod alebo výstup iónov tiež naznačuje pohyby zubnej vody v bunke, takže čerpadlo sa podieľa na regulácii objemu buniek.
- Generovanie potenciálu membrány: Vylúčenie 3 sodíkových iónov za každé 2 zavedené draslíkové ióny spôsobuje membránu. Tento rozdiel je známy ako odpočinkový potenciál.
Na+ má extracelulárnu koncentráciu asi 142 MEQ/L, zatiaľ čo jej intracelulárna koncentrácia je iba 12 mEq/l; Na druhej strane K+je v bunke koncentrovanejší (140 meq/l) ako mimo neho (4 meq/l).
Aj keď elektrický náboj týchto iónov neumožňuje ich prechod cez membránu, existujú iónové kanály, ktoré to umožňujú (selektívne), ktoré uprednostňujú pohyb, ak sú sily, ktoré sa bežne pohybujú tieto ióny.
Môže vám slúžiť: membránové receptory: funkcie, typy, ako fungujúTeraz majú tieto rozdiely v koncentrácii veľký význam v ochrana homeostázy organizmu a musí sa udržiavať v určitej rovnováhe, ktorá by sa stratila.
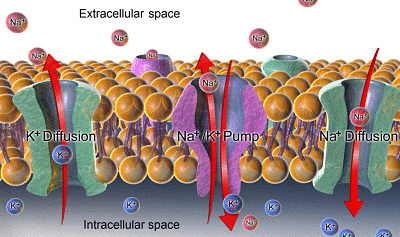 Šírenie a sodík draselného (zdroj: Bruceblaus. Pri použití tohto obrázka v externých zdrojoch je možné uviesť ako: Blausen.Zamestnanci COM (2014). „Medical Gallery of Blausen Medical 2014“. Wikijournal of Medicine 1 (2). Doi: 10.15347/WJM/2014.010. ISSN 2002-4436.Derivát Mikael Häggström/CC od (https: // creativecommons.Org/licencie/o/3.0) Via Wikimedia Commons)
Šírenie a sodík draselného (zdroj: Bruceblaus. Pri použití tohto obrázka v externých zdrojoch je možné uviesť ako: Blausen.Zamestnanci COM (2014). „Medical Gallery of Blausen Medical 2014“. Wikijournal of Medicine 1 (2). Doi: 10.15347/WJM/2014.010. ISSN 2002-4436.Derivát Mikael Häggström/CC od (https: // creativecommons.Org/licencie/o/3.0) Via Wikimedia Commons) - Rozdiel koncentrácie pre Na+ medzi vnútorným a mimo bunky vytvára chemický gradient, ktorý tlačí sodík dovnútra a spôsobuje, že tento ión neustále vstupuje a vkĺzne, aby rozptýlil tento rozdiel, to znamená, aby zodpovedal koncentráciám na oboch stranách.
- Gradient draslíka sa udržiava v opačnom smere, to znamená zvnútra von, ktorý umožňuje konštantný výkon iónu a jeho vnútorné redukcie a vonkajšie zvýšenie.
Funkcia čerpadla Na+/K+ umožňuje extrakciu sodíka, ktorý vstúpil difúziou prostredníctvom kanálov alebo inými transportnými trasami, a znovuzavedenie draslíka, ktorý bol šírený smerom von, čo umožňuje zachovanie intra a extracelulárnych koncentrácií týchto iónov.
Mechanizmus (proces)
Mechanizmus pôsobenia ATPázy Na+/K+ pozostáva z katalytického cyklu, ktorý znamená prenosové reakcie skupiny fosforyl (PI) a konformačné zmeny enzýmu, ktorý prechádza zo stavu E1 do štátu E2 a naopak.
Operácia vyžaduje prítomnosť ATP a Na+ vo vnútri bunky a K+ v extracelulárnej tekutine.
Spojenie sodíkových iónov pre transportér
Cyklus sa začína v stave konformácie E1 enzýmu, v ktorom sú 3 cytosolické miesta Na+ Únie a vysoká afinita (km 0,6 mm), ktoré sú úplne obsadené, pretože intra koncentrácia iónu (12 mM) jej umožňuje.
Hydrolýza ATP
V tomto stave (E1) a s Na+ pripevnenou na svoje miesta Únie je ATP pripevnený na svoje miesto v cytosolickom sektore molekuly, fosfátová skupina na 376 aspartátu sa prenáša a prenáša a tvorí vysoko energiu acilfosfátu, ktorý vyvoláva konformačná zmena na stav E2.
Vylúčenie 3 sodíkových iónov a zavedenie 2 iónov draslíka
Konformačná zmena v štáte E2 naznačuje, že miesta Na+ Únie prechádzajú do zahraničia, ich príbuznosť k iónu veľa klesá a uvoľňuje sa v extracelulárnej tekutine, zatiaľ čo zároveň príbuznosť miest Únie k K+ zvyšuje A tieto ióny sa viažu na čerpadlo.
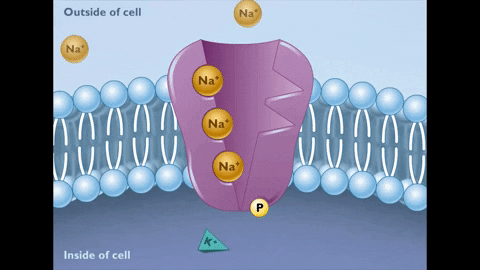 Počas stavu E2 sa ióny Na+ uvoľňujú na druhej strane membrány.
Počas stavu E2 sa ióny Na+ uvoľňujú na druhej strane membrány. 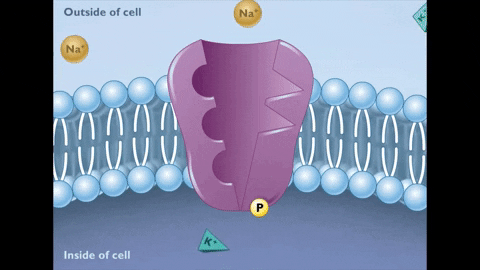 Tento nový stav pumpy zase vytvára afinitu k spojeniu K iónov+
Tento nový stav pumpy zase vytvára afinitu k spojeniu K iónov+ Zvrátenie z E2 do E1
Akonáhle sa uvoľní Na+ a K+ je zjednotený, hydrolýza aspartylového fosfátu sa vytvorí a konformačná zmena štátu E2 na štát E1 je zvrátená, s znovuzavedením miest Únie pre prázdne Na+ a K+ obsadené K+ obsadené K+.
Keď dôjde k tejto zmene, stránky pre Na+ obnovujú svoju afinitu a stránky K+, s ktorými sa K+ uvoľňuje vo vnútri bunky.
Dôležitosť
Pri udržiavaní bunkovej osmolarity
Bomba Na+/K+ bola prítomná vo väčšine, ak nie vo všetkých cicavčích bunkách, v ktorých má všeobecný význam tým, že prispieva k zachovaniu svojej osmolarity, a teda k objemu jej objemu.
Môže vám slúžiť: peroxidázy: Štruktúra, funkcie a typyNepretržitý vstup sodíkových iónov do bunky kondicionuje zvýšenie intracelulárneho počtu osmoticky aktívnych častíc, ktoré indukuje vstup vody a zvýšenie objemu, ktorý by skončil spôsobením prasknutia membrány a zrútenia buniek.
Pri tvorbe membránového potenciálu
Keď tieto čerpadlá zavádzajú iba 2 k+ za každé 3 Na+, ktoré vyberú, správajú sa elektrogeneticky, čo znamená, že „dekompenzujú“ vnútorné elektrické náboje, čo uprednostňuje výrobu charakteristického membránového potenciálu telesných buniek.
Jeho dôležitosť je zrejmá aj vo vzťahu k bunkám, ktoré tvoria excitačné tkanivá, v ktorých sa akčné potenciály vyznačujú vstupom iónu Na+, ktoré depolarizujú bunku, a výstup K+, ktorý ju repolarizuje.
Tieto iónové pohyby sú možné vďaka prevádzke čerpadiel Na+/K+, ktoré prispievajú k výrobe chemických gradientov, ktoré presúvajú príslušné ióny.
Bez týchto čerpadiel, ktoré fungujú v opačnom smere, by koncentračné gradienty týchto iónov rozptýlili a excitačná aktivita by zmizla.
Vo funkcii obličiek
Ďalším aspektom, ktorý zdôrazňuje extrémny význam bômb po sodíkovom draseri, je vo vzťahu k funkcii obličiek, čo by nebolo nemožné.
Funkcia ob.
Resorpcia sodíka, vody a mnohých filtrovaných látok závisí od týchto čerpadiel, ktoré sa nachádzajú v bazolaterálnej membráne buniek, ktoré tvoria epitel rôznych rúrkových segmentov obličkových nefronov.
Epitelové bunky, ktoré zväčšujú obličkové tubuly, majú tvár, ktorá je v kontakte so svetlom tubulu a ktorá sa nazýva apikálna tvár a ďalšia, ktorá je v kontakte s interstíciou okolo tubulu a nazýva sa bazolaterálne.
Voda a látky, ktoré sú reabsorbované.
Reabsorpcia Na+ je kľúčová vo vzťahu k nemu, ako aj vo vzťahu k vode a od iných látok, ktoré závisia od jeho. Apikálny vstup Na+ bunka vyžaduje, aby existoval gradient, ktorý ho pohybuje a ktorý znamená veľmi nízku koncentráciu iónu vo vnútri bunky.
Táto nízka intracelulárna koncentrácia Na+ je produkovaná sodíkovými pumpami z bazolaterálnej membrány, ktoré intenzívne pracujú na odstránení iónu z buniek do interstície.
Odkazy
- Ganong WF: Všeobecný a bunkový základ lekárskej fyziológie, v: Preskúmanie lekárskej fyziológie, 25. vydanie. New York, McGraw-Hill Education, 2016.
- Guyton AC, Hall Ji: Transport látok cez bunkovú membránu, In: Učebnica lekárskej fyziológie, 13. Ed, AC Guyton, JE Hall (eds). Philadelphia, Elsevier Inc., 2016.
- Lodish H, Berk A, Zipursky SL, Matsudaira P, Baltimore D, Darnell J: Transport cez bunkové membrány, In: Molekulárna a bunková biológia, 4. vydanie.
- Nelson, D. L., Lehninger, a. L., & Cox, M. M. (2008). Lehninger princípy biochémie. Macmillan.
- Alberts, b., Bray, D., Hopkin, k., Johnson, a. D., Lewis, J., Raff, m.,… & Walter, P. (2013). Základná bunková biológia. Girlandská veda.
- « Časti a funkcie charakteristík Soma
- Charakteristiky Mayates (Cotinis mutabiis), biotop, reprodukcia »

