Aldehydy
- 2374
- 93
- Tomáš Klapka
Čo sú aldehydy?
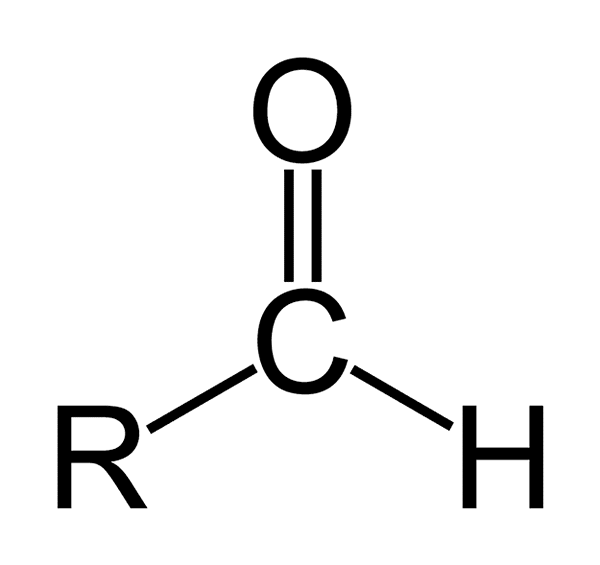
Ten aldehydy Sú to organické zlúčeniny, ktoré majú všeobecný vzorec rcho. R predstavuje alifatický alebo aromatický reťazec; C uhlík; Alebo kyslík a H vodík. Vyznačujú sa vlastnením karbonylovej skupiny, ako sú ketóny a karboxylové kyseliny, takže aldehydy sa tiež nazývajú karbonylové zlúčeniny.
Karbonylová skupina dáva aldehyde mnoho jeho vlastností. Sú to zlúčeniny, ktoré sa ľahko oxidujú a sú veľmi reaktívne na nukleofilné prídavky. Dvojitá väzba karbonylovej skupiny (C = O) predstavuje dva atómy, ktoré majú rozdiely v ich avidite elektrónmi (elektronegativita).
Kyslík priťahuje elektróny silnejšie ako uhlík, takže elektronický oblak sa pohybuje smerom k nemu tým, že vytvára dvojitú väzbu medzi uhlíkom a kyslíkom polárnej povahy, s dôležitým dipólovým momentom. To robí aldehydos.
Inými slovami, aldehydos sú typom organických zlúčenín vyplývajúcich z oxidácie určitých alkoholov.
Chemická štruktúra aldehydos
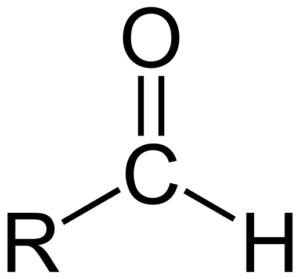 Chemická štruktúra aldehydos
Chemická štruktúra aldehydos Aldehydos pozostáva z karbonylu (c = o), s ktorým je atóm vodíka priamo prepojený. To ho odlišuje od iných organických zlúčenín, ako sú ketóny (r2C = o) a karboxylové kyseliny (RCOOH).
Horný obrázok zobrazuje molekulárnu štruktúru okolo -cho, skupinová formila. Kvalilná skupina je plochá, pretože uhlík a kyslík majú hybridizáciu SP2. Táto rovinnosť je náchylná na útok nukleofilových druhov, a preto je ľahko oxidovaná.
Čo znamená takáto oxidácia? K tvorbe spojenia s akýmkoľvek iným viac elektronegatívnym atómom ako uhlíkom; A v prípade aldehydos je to kyslík. Aldehyd teda oxiduje kyselinu karboxylovú, -COH. Čo keby sa aldehyd znížil? Namiesto toho by sa vytvoril primárny alkohol, ROH.
Aldehydos sa vyskytuje iba z primárnych alkoholov: tie, kde je skupina OH na konci reťazca. Podobne skupina formil vždy Je na konci reťazca alebo vyniká z nej alebo prsteň ako substituent (ak existujú ďalšie dôležitejšie skupiny, napríklad -cooh).
Fyzikálne a chemické vlastnosti aldehydov
Keďže sú polárne zlúčeniny, ich body topenia sú väčšie ako body nepolárnych zlúčenín. Aldehydos molekuly nie sú schopné viazať intermolekulárne vodíkovými mostmi, pretože iba atómy uhlíka sa spojili s atómami vodíka.
Z dôvodu vyššie uvedeného majú aldehydy nižšie body varu ako alkoholy a karboxylové kyseliny.
Fúzne body
Formaldehyd -92; Acetaldehyd -121; Propionaldehyd -81; n- butiraldehyd -99; N -valeraldehyd -91; Caproaldehyd -; Heptaldehyd - 42; Fenylacetaldehyd -; Benzaldehyd -26.
Body varu
Formaldehyd -21; Acetaldehyd 20; Propional Of -Hyd 49; N-Butiraldehido 76; N-Valleraldehyd 103; Caproaldehyd 131; Heptaldehyd 155; Fenylacetaldehyd 194; Benzaldehyd 178.
Môže vám slúžiť: konkrétne vlastnosti hmoty: Čo sú a príkladyRozpustnosť vo vode vyjadrená v G/100 g H2Ani
Formaldehyd, veľmi rozpustný; acetaldehyd, nekonečné; Propionaldehyd, 16; N-butiraldehyd, 7; N-valeraldehyd, mierne rozpustný; Caproaldehyd, mierne rozpustný; Fenylacetaldehyd mierne rozpustný; Benzaldehyd, 0,3.
Body varu aldehydov majú tendenciu sa priamo zvyšovať s molekulovou hmotnosťou. Naopak, existuje tendencia znižovať rozpustnosť aldehydov vo vode, keď sa zvyšuje ich molekulová hmotnosť. To sa odráža vo fyzických konštantách novo spomínaných aldehydov.
Reaktivita aldehydos
Oxidačná reakcia
Aldehydy môžu oxidovať zodpovedajúcu karboxylovú kyselinu v prítomnosti ktorejkoľvek z týchto zlúčenín: Ag (NH3)2, Kmno4 v poriadku2Cr2Ani7.
Redukcia na alkoholy
Môžu sa sami vodíkom pomocou katalyzátorov niklu, platiny alebo paladium. C = o sa teda transformuje na c-oh.
Redukcia na uhľovodíky
V prítomnosti Zn (Hg), koncentrovaného HCl alebo v NH2NH2 Aldehydos stratia karbonylovú skupinu a stanú sa uhľovodíkami.
Nukleofilný prírastok
Existuje niekoľko zlúčenín, ktoré sa pridávajú do karbonylovej skupiny, medzi nimi sú: Grignard, kyanidové činidlá, deriváty amoniaku a alkoholy.
Nomenklatúra Aldehydos
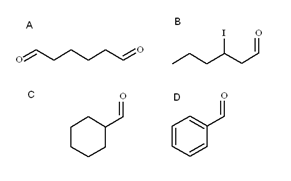 Štyri aldehydy. Zdroj: Gabriel Bolívar
Štyri aldehydy. Zdroj: Gabriel Bolívar Na vynikajúcom obrázku sú ilustrované štyri aldehydos. Ako sú pomenované?
Pretože sú hrdzavými primárnymi alkoholmi, názov alkoholu sa zmení na konci -ol od -al. Teda metanol (vyberte si3Och), ak je oxidovaný na Cho3Cho sa nazýva Metanal (formaldehyd); Chvály3Chvály2Cho Etanal (acetaldehyd); Chvály3Chvály2Chvály2Cho Propanal a Cho3Chvály2Chvály2Chvály2Butanal Cho.
Všetky novo pomenované Aldehydos majú skupinu -cho na konci reťazca. Keď je to na oboch koncoch, ako v A, na konci -k nemu sa pridá predpona DI-. Rovnako ako šesť uhlíkov (počítanie oboch formylových skupín), odvodzuje od 1-hexanolu, a jeho názov je preto: hexánvytočiť.
Ak je substituent, ako napríklad alquilický radikál, dvojité alebo trojité spojenie alebo halogénové uhlíky hlavného reťazca, sú uvedené v uvedení čísla 1. Teda aldehyd B sa nazýva: 3-jodhexanal.
Avšak v aldehydoch C a D nemá skupina -cho žiadnu prioritu na identifikáciu týchto zlúčenín ostatných. C je cykloalcano, zatiaľ čo d a benzén, obidve s jedným z jeho H nahradeným skupinou formila.
V nich, keďže hlavná štruktúra je cyklická, sa skupina formil pomenuje karbaldehyd. C je teda cyklohexanokbaldehyd a d benzenokarbaldehyd (lepšie známy ako benzaldehyd).
Použitie aldehydos
V prírode sú aldehydy schopné udeliť príjemné príchute, ako je prípad cinnamaldehydu, zodpovedný za charakteristickú chuť škorice. Preto sa zvyčajne používajú ako umelé arómy v mnohých výrobkoch, ako sú sladkosti alebo jedlo.
Formaldehyd
Formaldehyd je aldehyd, ktorý sa vyskytuje priemyselne vo väčšom množstve. Formaldehyd získaný oxidáciou metanolu sa používa v 37% roztoku plynu vo vode pod názvom formalín. Používa sa to pri opaľovaní kože a na ochranu a balzamovanie mŕtvol.
Môže vám slúžiť: octanu sodný: štruktúra, vlastnosti, syntéza, použitieFormaldehyd sa používa aj ako germicid, fungicíd a insekticíd pre rastliny a zeleninu. Jeho najväčšou užitočnosťou je však príspevok k výrobe polymérneho materiálu. Plast nazývaný Bakelita je syntetizovaný reakciou medzi formaldehydom a fenolom.
Bakelita
Bakelita je veľká tvrdá -hardová -rozmerová štruktúra polyméru používaná v mnohých domácich náter, ako sú hrnce, panvice, kávovary, nože atď.
Polyméry podobné bakelita sú vyrobené z formaldehydu v kombinácii s močovinou a zlúčeninami melamínu. Tieto polyméry sa používajú nielen ako plasty, ale používajú sa aj ako lepiace tyčinky a poťahový materiál.
Preglejka
Preglejka je komerčný názov materiálu tvoreného tenkým listom dreva, ktoré sa spojili polymérmi vyrobenými z formaldehydu. Formic a Melmac Brands sa vyrábajú s účasťou na tomto. Formika je plastový materiál používaný v nábytkovom povlaku.
Plast MMLMAC sa používa pri vypracovaní dosiek, pohárov, šálok atď. Formaldehyd je surovina pre syntézu zlúčeniny metylén-difenil-diizociátu (MDI), prekurzor polyuretánu.
Polyuretán
Polyuretán sa používa ako izolátor v chladničkách a mrazničkách, vyplnený na nábytok, matrace, povlaky, lepidlá, podrážky atď.
Butiraldehyd
Butiraldehyd je hlavným predchodcom syntézy 2-etylhexanolu, ktorý sa používa ako plastifikátor. Má príjemnú jablkovú arómu, ktorá umožňuje jeho použitie v potravinách ako aróma.
Používa sa tiež pre gumové urýchľovače. Pri výrobe rozpúšťadiel zasahuje ako medziprodukčné činidlo.
Acetaldehyd
Acetaldehyd sa použil pri produkcii kyseliny octovej. Ale táto funkcia acetaldehydu sa znížila dôležitosť, pretože bola vysídlená procesom karbontalácie metanolu.
Syntéza
Ďalšími aldehydmi sú prekurzory oxoalkoholov, ktoré sa používajú pri výrobe detergentov. So -caled Oxoalkoholy sa pripravujú pridaním oxidu uhoľnatého a vodíka do olefínu, aby sa získal aldehyd. A nakoniec aldehyd je vodík na získanie alkoholu.
Niektoré aldehydos sa používajú pri výrobe parfumov, ako je napríklad Chanel č. 5. Mnoho prírodných aldehydov má napríklad príjemné pachy, napríklad: Heptanal má vôňu zelenej trávy; Octanal, zápach oranžovej; Nonanal, vôňa ruží a citralovej vône Limy.
Príklady aldehydov
Glutaraldehyd
 Glutaraldehyd. Zdroj: Jynto [CC0], z Wikimedia Commons
Glutaraldehyd. Zdroj: Jynto [CC0], z Wikimedia Commons Glutaraldehyd predstavuje vo svojej štruktúre dve formy skupiny na oboch koncoch.
Predávkovaný pod názvom Cidex alebo Glutararal sa používa ako dezinfekčný prostriedok na sterilizáciu chirurgických nástrojov. Používa sa pri čistení bradavíc na chodidlách, ktoré sa nanáša ako tekutina.
Používa sa tiež ako látky na fixačné látky v histologických a patologických laboratóriách.
Môže vám slúžiť: sulfát meďnatého (CUSO4): Štruktúra, vlastnosti, získanie, použitiaBenzaldehyd
Je to najjednoduchší aromatický aldehyd, ktorý je tvorený benzénovým krúžkom, kde je prepojená skupina formil.
Nachádza sa v mandľovom oleji, a preto jeho charakteristická vôňa, ktorá umožňuje jeho použitie ako ochutenie potravín. Okrem toho sa používa pri syntéze organických zlúčenín súvisiacich s výrobou liekov a plastov.
Glyceraldehyd
Je to aldotriosa, cukor predstavovaný tromi atómami uhlíka. Predstavuje dva izoméry, ktoré sa nazývajú d a l enantioméry. Glyceraldehyd je prvý monosacharid získaný vo fotosyntéze počas temnej fázy (Calvin Cycle).
Glyceraldehyd-3-fosfát
 Glyceraldehyd. Zdroj: Jynto a Ben Mills
Glyceraldehyd. Zdroj: Jynto a Ben Mills Na vynikajúcom obraze je ilustrovaná štruktúra glyceraldehyd-3-fosfátu. Červené gule vedľa žltej zodpovedajú fosfátovej skupine, zatiaľ čo čierna k uhlíkovej kostre. Červená guľa spojená s blankou je skupina OH, ale keď je čierna guľa spojená a druhá s bielym, potom je to skupina Cho.
Glyceraldehyd-3-fosfát zasahuje do glykolýzy, metabolického procesu, v ktorom sa glukóza degraduje na kyselinu pyruvovu výrobou ATP, energetickej rezervoáru živých bytostí živých bytostí. Okrem produkcie NADH, biologické redukčné činidlo.
V glykolelelehyd-3-fosfátovom glykolýze a fosfátový dihydroacetón sú spôsobené D-Frucease-6-6-6-Bifary-fosfát.
Glyceraldehyd-3-fosfát zasahuje do metabolického procesu známeho ako pentózový cyklus. V tomto je generovaný NADPH, dôležitý biologický reduktor.
11 -cis -retinálny
 11 -cis -retinálny
11 -cis -retinálny P-karotén je prírodný pigment prítomný v niekoľkých zelenine, najmä v mrkve. Zažiť oxidačný zlom v pečeni, a tak sa transformovať v retinolovom alkoholu alebo vitamíne A. Oxidácia vitamínu A a následná izomerizácia jednej z jeho dvojitých väzieb tvorí 11-cis-retinálny aldehyd.
Pyridoxálny fosfát (vitamín B6)
 Pyridoxálny fosfát alebo vitamín B6. Zdroj: Jynto a Ben Mills.
Pyridoxálny fosfát alebo vitamín B6. Zdroj: Jynto a Ben Mills. Je to protetická skupina pripojená k niekoľkým enzýmom, čo je aktívna forma vitamínu B6 a podieľa sa na procese syntézy inhibičného neurotransmitera GABA.
Kde je formilová skupina vo svojej štruktúre? Všimnite si, že sa to líši od ostatných skupín spojených s aromatickým krúžkom.
Salicilaldehyd
Je to surovina pre syntézu kyseliny acetylsalicylovej, analgetickej a antipyretickej medicíny známa ako aspirín.
Odkazy
- Robert C. Neuman, Jr. Kapitola 13, karbonylové zlúčeniny: ketóny, aldehydy, karboxylové kyseliny. [PDF]. Prevzaté z: chem.Ucr.Edu
- Germán Fernández. (14. september 2009). Nomenklatúra Aldehydos. Prevzaté z: chemicicaorganica.slepo
- Tón.W. Graham Solomons, Craight B. Fryhle. Organická chémia. (Desiate vydanie, s. 729-731) Wiley Plus.
- Jerry March a William H. Hnedý. (31. decembra 2015). Aldehyd. Zobraté z: Britannica.com
- Wikipedia. (2018). Aldehydy. Prevzaté z: https: // in.Wikipedia.orgi/aldehyd
- Morrison, r. Tón. A Boyd, r. N. (1990). Organická chémia piate vydanie. Redakcia Addison-Wesley Iberoamericana.
- Carey, f. Do. (2006). Organická chémia šieste vydanie. Redakcia MC Graw Hill.
- Mathews, ch. Klimatizovať., Van Holde, K. A. A Athern, K. G. (2002). Biochémia. Tretia edícia. Redakcia Pearson Adisson Wesley.

