Štruktúra izoamilo, vlastnosti, syntéza a používa acetát

- 5154
- 834
- Blažej Hrmo
On Octy Je to ester, ktorého molekulárny vzorec je Cho3Coo (ch2)2Chváli3)2. Pri izbovej teplote pozostáva z mastného, číreho, bezfarebného, horľavého a prchavého tekutiny. V skutočnosti je to príliš prchavý a voňavý ester.
Jeho hlavnou charakteristikou je rozlúčiť sa s vôňou, ktorá prispieva k aróme mnohých plodov, najmä v banáne alebo banánom. Toto posledné ovocie tiež predstavuje jeden z jeho prírodných zdrojov par excellence.
 Banány, ktorých charakteristická aróma je spôsobená acetátom izoamilo. Zdroj: Pixabay.
Banány, ktorých charakteristická aróma je spôsobená acetátom izoamilo. Zdroj: Pixabay. Odtiaľ názov banánového oleja, ktorý sa udeľuje roztoku octanu izoamil alebo zmesi izomylacetátu s nitrocelulózou. Zlúčenina sa široko používa ako chuť jedla, zmrzliny a sladkostí.
Okrem toho sa používa pri vypracovaní vôní s rôznymi pracovnými miestami. Je to tiež rozpúšťadlo, ktoré sa používa pri extrakcii kovov a organických zlúčenín, ako je kyselina octová.
Izoamilo acetát je výsledkom sterifikácie izoamylalalkoholu s kyselinou octovou. V laboratóriách vyučovania v organickej chémii predstavuje táto syntéza zaujímavú skúsenosť na implementáciu esterifikácie, zatiaľ čo povodne laboratórium banánovou vôňou.
[TOC]
Štruktúra octanu izoamilo
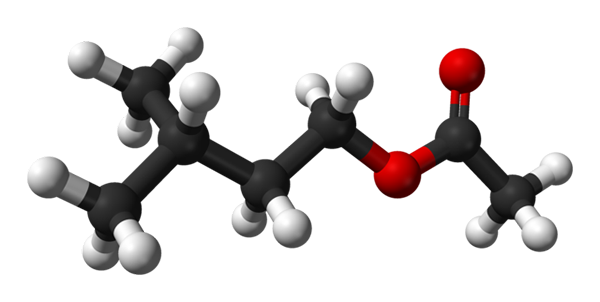 Štruktúra octanu izoamilo. Zdroj: Ben Mills [verejná doména]
Štruktúra octanu izoamilo. Zdroj: Ben Mills [verejná doména] Na hornom obrázku máte molekulárnu štruktúru acetátu izoamilu pomocou modelu guľôčok a stĺpcov. Červené gule zodpovedajú atómom kyslíka, konkrétne tým, ktoré identifikujú túto zlúčeninu ako ester; jeho časť éteru, r-O-r a karbonylovej skupiny, c = o, potom má štrukturálny vzorec r'Coor.
Vľavo, r', Máte izopentilný alkyglický radikál (Cho3)2Štiepka2Chvály2; A vpravo, r, do metylovej skupiny, na ktorú je dlžný „acetát“ mena tohto esteru. Je to relatívne malý ester, schopný interagovať s chemickými receptormi zápachu našich nosov, čo spôsobuje signály, ktoré mozog interpretuje ako vôňa.
Môže vám slúžiť: rozvetvené alkányIntermolekulárne interakcie
Samotná molekula izoamilu acetátu je flexibilná; Radikál Izopentil však neprináša úžitok medzimolekulárne interakcie, pretože je rozvetvený, čo stericky bráni atómom kyslíka, aby účinne interagovali dipól-dipolo sily.
Tieto dva kyslíky tiež nemôžu akceptovať vodíkové mosty; Štrukturálne molekula nemá, ako ich darovať. Izoamilový acetát, ktorý sa týka prerušených dipólov, môže intermolekulárne interagovať prostredníctvom londýnskych disperzných síl; ktoré sú priamo úmerné ich molekulárnej hmotnosti.
Je to teda molekulárna hmotnosť esteru zodpovedného za jeho molekuly, aby vytvorila kvapalinu s vysokým bodom varu (141 ° C). Podobne je zodpovedný za svoj tuhý kryt na teplotu -78 ° C.
Banánová vôňa
Jeho medzimolekulárne sily sú také slabé, že tekutina je dostatočne prchavá na to, aby prenikla do svojho okolia s vôňami banánov. Je zaujímavé, že sladká vôňa tohto esteru sa môže zmeniť, ak sa počet uhlíkov zníži alebo zvýši.
To znamená, že ak namiesto toho, aby mal šesť alifatických uhlíkov, mal päť (s radikálnou izobutil), jeho vôňa by sa podobala vône maliny; Keby bol radikál secbutil, zápach by bol naložený stopami organických rozpúšťadiel; A keby som mal viac ako šesť uhlíkov, vôňa by sa začala stať mydlom a kovovým.
Vlastnosti
Chemické názvy
-Octy
-Izopentilný etanoát
-3-metylbutilo acetát
-Izopentilo acetát
-Banánový olej alebo banán.
Molekulárna receptúra
C7H14Ani2 alebo CH3Coo (ch2)2Chváli3)2
Molekulová hmotnosť
130 187 g/mol.
Fyzický popis
Je to mastná, čistá a bezfarebná tekutina.
Vôňa
Pri izbovej teplote má intenzívny a príjemný zápach banánov.
Príchuť
Má príchuť podobnú príchute, ktorú predstavujú hruška a jablko.
Bod varu
124,5 ° C.
Bod topenia
-78,5 ° C.
zapaľovač
92 ° F zatvorená šálka (33 ° C); Šálka otvorená 100 ° F (38 ° C).
Môže vám slúžiť: kryštalické tuhé látky: štruktúra, vlastnosti, typy, príkladyRozpustnosť
2.000 mg/l A 25 ° C.
Rozpustnosť v organických rozpúšťadlách
Misilné s alkoholom, éterom, etylacetátom a amylalkoholom.
Hustota
0,876 g/cm3.
Hustota
4,49 (vo vzťahu vzduchu = 1).
Tlak vodnej pary
5,6 mmHg pri 25 ° C.
Teplota
680 ° F (360 ° C).
Hrebeň
-1,03 CPoise pri 8,97 ° C
-0,872 CPoise pri 19,91 ° C.
Spaľovacie teplo
8.000 limet/g.
Prah
Vzduch = 0,025 ul/l
Voda = 0,017 mg/l.
Index lomu
1 400 až 20 ° C.
Relatívna rýchlosť odparovania
0,42 (vo vzťahu k butylacetátu = 1).
Dialektrická konštanta
4,72 až 20 ° C.
Ukladanie
Izoamilo acetát je horľavá a prchavá zlúčenina. Preto musí byť zima v úplne hermetických nádobách, zďaleka horľavých látok.
Syntéza
Vyrába sa esterifikáciou izoamylalalkoholu s ľadovskou kyselinou octovou v procese známeho ako Fisherova estterifikácia. Kyselina sírová sa zvyčajne používa ako katalyzátor, ale aj kyselina p-toluenosulfónová katalyzuje reakciu:
(Ch3)2CH-CH2-Chvály2Chvály2Oh + ch3Cooh => ch3Kočiary2-Chvály2-Chvály2-Chváli3)2
Žiadosti
Príchuť jedla a nápojov
Používa sa na udelenie hruškovej príchute vo vode a sirupoch. Používa sa v Číne na prípravu ovocných príchutí, ako sú jahody, Blackberry, ananás, hruška, jablko, hrozno a banán. Použité dávky sú: 190 mg/kg v cukrárni; 120 mg/kg v pečive; 56 mg/kg v zmrzline; a 28 mg/kg v nealkoholických nápojoch.
Rozpúšťadlo a riedidlo
Je to rozpúšťadlo pre:
-Nitrocelulóza a celululoid
-Vodotesné lak
-Ester gumy
-Vinylová živica
-Cummarona živica a ricínový olej.
Používa sa ako rozpúšťadlo na stanovenie chrómu a používa sa ako extrakčné činidlo železa, kobaltu a niklu. Používa sa tiež ako rozpúšťadlo olejomaľieb a starých lakquerov. Okrem toho sa používa pri vypracovaní laku na nechty.
Tento ester sa používa ako riedidlo pri produkcii kyseliny octovej. Olej sa používa ako surovina v oxidačnom procese, ktorý produkuje vodný roztok kyseliny octovej a iných zlúčenín, ako je kyselina mravčová a kyselina propiónová.
Môže vám slúžiť: etylénglykol: Vlastnosti, chemická štruktúra, použitieAko rozpúšťadlo a nositeľ iných látok sa použil na začiatku leteckého priemyslu na ochranu tkanín pred vzduchovými krídlami.
Vône
-Používa sa ako atmosféra na zakrytie zápachov.
-Používa sa ako parfum v topánkach.
-Na preukázanie účinnosti antigázových masiek, pretože izoamilový acetát má veľmi nízku prahovú hodnotu zápachu a nie je príliš toxický.
-Používa sa vo vôňoch, ako je napríklad Chipre; mäkká aróma Osmanthus; Jacinto; a silná orientálna príchuť, ktorá sa používa v nízkych dávkach, nižšia ako 1%.
Ďalší
Používa sa pri vypracovaní hodvábu a umelých perly, fotografických filmov, nepremokavých a bronzujúcich lakov. Používa sa tiež v textilnom priemysle pri farbení a dokončení. Používa sa pri suchom umývaní oblečenia a látkového nábytku.
Okrem toho sa izoamilo acetát používa v rozpracovaní Rayonu, syntetickej tkaniny; Pri extrakcii penicilínu a ako štandardná chromatografická látka.
Riziká
Octajský izoamilo môže dráždiť pokožku a oči fyzickým kontaktom. Vdýchnutie môže spôsobiť podráždenie nosa, hrdlo a pľúca. Medzitým môže expozícia vysokým koncentráciám spôsobiť bolesti hlavy, ospalosť, závraty, závraty, únava a mdloby.
Predĺžený kontakt s pokožkou môže spôsobiť suchosť a praskanie.
Odkazy
- Bilbrey Jenna. (30. júla 2014). Izoamylacetát. Svet chémie Kráľovskou spoločnosťou chémie. Získané z: Chemistryworld.com
- Národné centrum pre biotechnologické informácie. (2019). Izoamylacetát. Databáza pubchem. Získané z: pubchem.Ncbi.NLM.NIH.Vláda
- Wikipedia. (2019). Izoamylacetát. Zdroj: In.Wikipedia.orgán
- Kráľovská spoločnosť chémie. (2015). Izoamylacetát. Chempider. Obnovený z: ChemSpider.com
- Ministerstvo zdravotníctva v New Jersey a služby seniorov. (2005). Izoamylacetát. [PDF]. Získané z: NJ.Vláda
- Chemická kniha. (2017). Izoamylacetát. Obnovené z: Chemicalbook.com
- « 4 obdobia chémie z praveku až do dnešného dňa
- Charakteristiky politickej reči, typy, problémy a príklady »

