Štruktúra trinitrotolueno (TNT), vlastnosti, použitie, riziká, výbuch

- 3656
- 708
- Ing. Ervín Petruška
On Trinitrotoluén Je to organická zlúčenina tvorená uhlíkom, kyslíkom, vodíkom a dusíkom s tromi nitro skupinami -NO2. Jeho chemický vzorec je C6H2(Ch3) (Nie2)3 alebo tiež kondenzovaný vzorec C7H5N3Ani6.
Jeho celé meno je 2,4,6-trinitrotoluén, ale bežne sa nazýva TNT. Je to kryštalická biela tuhá látka, ktorá môže explodovať pri zahrievaní nad určitou teplotou.
 2,4,6-trinitrotoluén kryštály, TNT. Wremmerswaal [CC BY-SA (https: // creativeCommons.Org/licencie/By-SA/4.0)]. Zdroj: Wikimedia Commons.
2,4,6-trinitrotoluén kryštály, TNT. Wremmerswaal [CC BY-SA (https: // creativeCommons.Org/licencie/By-SA/4.0)]. Zdroj: Wikimedia Commons. Prítomnosť v trinitrotoluéne z troch skupín nitro -not2 uprednostňuje skutočnosť, že s istotou exploduje. Preto sa široko používa v výbušných artefaktoch, projektiloch, bombách a granátoch.
Používa sa tiež na vykonávanie podvodných výbuchov, v hlbokých studniach a na výbuchy priemyselných alebo neohnutí.
TNT je jemný produkt, ktorý môže tiež využiť veľmi silné údery. Je to tiež toxické pre ľudské bytosti, zvieratá a rastliny. Miesta, kde sa vyskytli výbuchy.
Forma, ktorá môže byť účinná a ekonomická na zníženie koncentrácie v kontaminovanom prostredí TNT, je použitie niektorých typov baktérií a húb.
[TOC]
Chemická štruktúra
2,4,6-trinitrotoluén sa skladá z molekuly toluénu M6H5-Chvály3, ku ktorému boli pridané tri nitro skupiny -nie2.
Tri skupiny nitro -no2 Nachádzajú sa symetricky v benzénovom kruhu toluénu. Nachádzajú sa v pozíciách 2, 4 a 6, kde poloha 1 zodpovedá metylu -ch3.
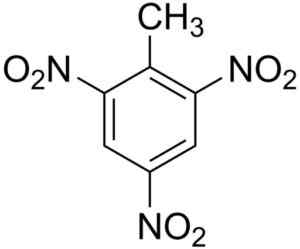 Chemická štruktúra 2,4,6-trinitrotoluénu. EDGAR181 [verejná doména]. Zdroj: Wikimedia Commons.
Chemická štruktúra 2,4,6-trinitrotoluénu. EDGAR181 [verejná doména]. Zdroj: Wikimedia Commons. Menovanie
- Trinitrotoluén
- 2,4,6-trinitrotoluén
- TNT
- Trilita
- 2-metyl-1,3,5-trinitobenzén
Vlastnosti
Fyzický stav
Kryštalická tuhá až bledožltá. Kryštály s ihlou.
Molekulová hmotnosť
227,13 g/mol.
Bod topenia
80,5 ° C.
Bod varu
Nevarte. Rozkladá sa výbuchom pri 240 ° C.
Bod vzplanutia
Nie je možné to zmerať, pretože exploduje.
Hustota
1,65 g/cm3
Rozpustnosť
Takmer nerozpustné vo vode: 115 mg/l A 23 ° C. Veľmi málo rozpustné v etanole. Veľmi rozpustný v acetóne, pyridíne, benzéne a toluéne.
Môže vám slúžiť: materiálne systémyChemické vlastnosti
Pri zahrievaní sa dá rozbiť výbušne. Po dosiahnutí 240 ° C exploduje. Môžete tiež explodovať, keď trpíte veľmi silnými údermi.
Pri zahrievaní až do rozkladu produkuje toxické plyny z oxidov dusíka nieX.
Proces výbuchu TNT
Výbuch TNT znamená chemickú reakciu. V podstate ide o proces spaľovania, v ktorom sa energia uvoľňuje veľmi rýchlo. Okrem toho sú emitované plyny, ktoré sú činidlami na prenos energie.
 TNT exploduje ľahko, keď sa zahrieva nad 240 ° C. Autor: OpenClipart-vektory. Zdroj: Pixabay.
TNT exploduje ľahko, keď sa zahrieva nad 240 ° C. Autor: OpenClipart-vektory. Zdroj: Pixabay. Aby sa vyskytla spaľovacia reakcia (oxidácia), musí byť prítomné palivo a oxidata.
V prípade TNT sa obidve nachádzajú v rovnakej molekule, pretože atómy uhlíka (C) a vodík (H) sú palivá a oxidant je kyslík (O) nitro skupín -No2. To umožňuje rýchlejšiu reakciu.
Oxidačná reakcia TNT
Počas spaľovacej reakcie TNT sú atómy zadné a kyslík (O) je bližšie k uhlíkovi (C). Okrem toho dusík -n nie2 Je redukovaný a stáva sa plynným dusíkom n2 čo je oveľa stabilnejšia zlúčenina.
Chemická reakcia výbuchu TNT možno zhrnúť takto:
2 c7H5N3Ani6 → 7 CO ↑ + 7 C + 5 h2Alebo ↑ + 3 n2↑
Uhlík sa vyskytuje (C) počas výbuchu vo forme čierneho oblaku a tiež sa vytvára oxid uhoľnatým (CO), čo je preto, že v molekule nie je dostatok kyslíka na úplné oxidovanie všetkých atómov uhlíka (C) a vodíka ( h) prítomný.
Získanie TNT
TNT je zlúčenina pripravená iba umelo ľudskou bytosťou.
V prostredí sa prirodzene nenachádza. Vyskytuje sa iba v niektorých vojenských zariadeniach.
Je pripravený dusičnanou toluénu (c6H5-Chvály3) So zmesou kyseliny dusičnej HNO3 a kyselina sírová H2SW4. Najprv zmes orto- a pre-Nitrotoliáni, ktorí ďalším energetickým nitrálnym tvoria symetrický trinitrotoluén.
Môže vám slúžiť: citrát sodný (C6H5O7NA3): Štruktúra, použitie, vlastnostiTNT používa
Vo vojenských činnostiach
TNT je výbušnina, ktorá sa používa vo vojenských zariadeniach a vojenských výbuchoch.
 Ručné granáty môžu obsahovať TNT. Autori: Materialscientist, Nemo5576 a TRONNO. Zdroj: Wikimedia Commons.
Ručné granáty môžu obsahovať TNT. Autori: Materialscientist, Nemo5576 a TRONNO. Zdroj: Wikimedia Commons. Používa sa na vyplnenie projektilov, granátov a vzduchových čerpadiel, pretože je dostatočne necitlivý na dopad prijatý na vystúpenie z dela pištole, ale môže explodovať, keď bude ovplyvnený výbuchom mechanizmom.
 Vzduchové bomby môžu obsahovať TNT. Autor: Christian Wittmann. Zdroj: Pixabay.
Vzduchové bomby môžu obsahovať TNT. Autor: Christian Wittmann. Zdroj: Pixabay. Nie je navrhnutý tak, aby vytvoril významnú fragmentáciu alebo spustenie projektilov.
V priemyselných aplikáciách
Používa sa na výbuchy priemyselného záujmu, na výbuch pod vodou (kvôli svojej nerozpustnosti vo vode) a hlbokých výbuchov. V minulosti sa používalo častejšie na demolácie. V súčasnosti sa používa spolu s inými zlúčeninami.
 Fotka výsledku výbuchu na zbúranie skaly v roku 1912. V tom čase sa TNT použil pri otryskaní, ktoré sa vyžadujú napríklad na otvorené železničné cesty. Obrázky knihy Internet Archive [Žiadne obmedzenia]. Zdroj: Wikimedia Commons.
Fotka výsledku výbuchu na zbúranie skaly v roku 1912. V tom čase sa TNT použil pri otryskaní, ktoré sa vyžadujú napríklad na otvorené železničné cesty. Obrázky knihy Internet Archive [Žiadne obmedzenia]. Zdroj: Wikimedia Commons. Bol tiež sprostredkovateľom pre farby a fotografické chemikálie.
Riziká
Môže explodovať, ak je vystavená intenzívnemu tepla, ohňu alebo veľmi silným úderom.
Je to dráždivé oko, pokožka a dýchací trakt. Je to veľmi toxická zlúčenina pre človeka aj zvieratá, rastliny a mnoho mikroorganizmov.
Medzi príznaky expozície TNT patrí bolesť hlavy, slabosť, anémia, toxická hepatitída, cyanóza, dermatitída, poškodenie pečene, konjunktivitída, nedostatok chuti do jedla, nevoľnosť, zvracanie, hnačka.
Je to mutagén, ktorý môže zmeniť genetické informácie (DNA) organizmu spôsobujúceho zmeny, ktoré môžu súvisieť s výskytom dedičných chorôb.
Bol tiež klasifikovaný ako generátor karcinogénu alebo rakoviny.
Znečistenie životného prostredia s TNT
TNT bola zistená v pôdach a vode v oblastiach vojenských vojnových operácií, na miestach výroby munície a kde sa vykonávajú vojenské výcvikové operácie.
Môže vám slúžiť: kyselina sorbová: štruktúra, vlastnosti, použitia, reakcie Pôdy a vody vojenských zón alebo vojenských operácií boli kontaminované TNT. Autor: Michael Gaida. Zdroj: Pixabay.
Pôdy a vody vojenských zón alebo vojenských operácií boli kontaminované TNT. Autor: Michael Gaida. Zdroj: Pixabay. Kontaminácia TNT je nebezpečná pre život zvierat, ľudských bytostí a rastlín. Aj keď sa TNT v súčasnosti používa v nižšom kvantovom.
Preto je jedným z najviac prispievajúcich k znečisteniu životného prostredia.
Riešenie kontaminácie TNT
Potreba „vyčistiť“ regióny kontaminované TNT motivovalo rozvoj niekoľkých nápravných procesov. Náprava je odstránenie znečisťujúcich látok na životné prostredie.
Náprava baktériami a hubami
Mnoho mikroorganizmov je schopných bioremediálneho TNT ako napríklad rodové baktérie Pseudomonas, Enterobakter, Mycobacterium a Clostridium.
Zistilo sa tiež, že existujú určité baktérie, ktoré sa vyvinuli na miestach kontaminovaných TNT a ktoré môžu prežiť a tiež degradovať alebo metabolizovať ako zdroj živín.
Ten Escherichia coli Napríklad preukázala vynikajúcu biotransformačnú kapacitu TNT, pretože má na ňu viac enzýmov, čo dokazuje toxicitu s vysokou toxicitou s vysokou toxicitou.
Okrem toho niektoré druhy húb môžu biotransformovať TNT, čím sa stanú neohrozenými minerálmi.
Nápravné subjekty s riasami
Na druhej strane niektorí vedci zistili, že riasy Spirulina Má schopnosť adsorbovať sa na povrchu jej buniek a asimilovať až 87% TNT prítomných vo vodách kontaminovaných touto zlúčeninou.
Tolerancia týchto rias voči TNT a jej schopnosť čistiť kontaminovanú vodu tým naznačujú vysoký potenciál týchto rias ako fytoremediátor.
Odkazy
- Alebo.Siež. Lekárska knižnica. (2019). 2,4,6-trinitrotoluén. Obnovený z pubchem.Ncbi.NLM.NIH.Vláda.
- Murray, s.G. (2000). Výbušniny. Mechanizmus výbuchu. V encyklopédii forenzných vied 2000, strany 758-764. Zotavené z vedeckých pracovníkov.com.
- Adamia, G. a kol. (2018). O možnosti aplikácie rias spirulina na fytoremediáciu vody znečistenej 2,4,6-trinitrotoluénom. Annals of Agranian Science 16 (2018) 348-351. Obnovené od čitateľa.Elsevier.com.
- Serrano-González, m.A. a kol. (2018). Biotransformácia a degradácia 2,4,6-trinitrotoluénu mikrobiálnym metabolizmom a ich interakcia. Obranná technológia 14 (2018) 151-164. PDF sa získal.Vedecké výrobky.com.
- Iman, m. a kol. (2017). Systémový biologický prístup k bioremediácii nitroaromatiky: Analýza obmedzení založená na obmedzení biotransformácie 2,4,6-trinitrotoluénu pomocou Escherichia coli. Molekuly 2017, 22, 1242. MDPI sa zotavila.com.
- Windholz, m. a kol. (redaktori) (1983). Index Merck. Enyklopedia chemikálií, liekov a biologických. Desiate vydanie. Merck & Co., Inc.
- Morrison, r.Tón. a Boyd, r.N. (2002). Organická chémia. 6. vydanie. Hara.
- « Kultúrna antropológia Objekt štúdie, história, metodika
- Kultúra brazílskych tradícií, zvykov, gastronómie, hudby, náboženstva »

