Čo sú anóda a katóda?

- 2751
- 877
- Alan Milota
On anóda a katóda Sú to typy elektród nachádzajúcich sa v elektrochemických bunkách. Jedná sa o zariadenia schopné vyrábať elektrinu chemickou reakciou. Najpoužívanejším elektrochemickým bunkám sú batérie.
Existujú dva typy elektrochemických buniek, elektrolytických buniek a galvanických alebo voltaických buniek. V elektrolytických bunkách sa chemická reakcia produkovaná energiou nedochádza spontánne, ale elektrický prúd sa transformuje na chemickú oxidačnú reakciu.

Galvanická bunka sa skladá z dvoch semi -lodgs. Sú spojené dvoma prvkami, kovovým vodičom a soľným mostom.
Elektrický vodič, ako je uvedené podľa jeho mena, vedie elektrinu, pretože má veľmi malý odpor voči pohybu elektrického náboja. Najlepší vodiči sú zvyčajne kovy.
Salínsky most je trubica, ktorá spája dva semi -llady, pričom si zachováva elektrický kontakt a bez toho, aby sa komponenty každej bunky pripojili.Každá semi -stredná galvanická bunka obsahuje elektródu a elektrolyt.
Keď dôjde k chemickej reakcii, jeden zo semilladov stráca elektróny na svoju elektródu prostredníctvom oxidačného procesu; Zatiaľ čo ostatné vyhrávajú elektróny pre elektródu, prostredníctvom procesu redukcie.
Oxidačné procesy sa vyrábajú v anóde a redukčné procesy v katóde
[TOC]
Anóda
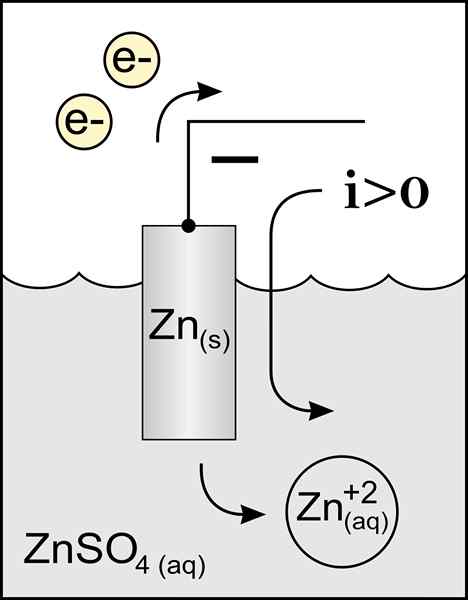 Diagram zinkovej anódy v voltaickej bunke. Zdroj: Originálna práca: Súbor: Zinková anóda 2.PNG od používateľa: Micheljullian (talk) Derivát Work: KES47/CC BY-S (http: // creativecommons.Org/licencie/By-SA/3.0/)
Diagram zinkovej anódy v voltaickej bunke. Zdroj: Originálna práca: Súbor: Zinková anóda 2.PNG od používateľa: Micheljullian (talk) Derivát Work: KES47/CC BY-S (http: // creativecommons.Org/licencie/By-SA/3.0/) Názov anódy pochádza z gréckeho ανά (Aná): hore a οδός (odós): cesta. Faraday bol ten, kto tento termín razil v devätnástom storočí.
Najlepšia definujúca anóda je elektróda, ktorá stráca elektróny pri oxidačnej reakcii. Normálne je spojená s pozitívnym pólom tranzitu elektrického prúdu, ale nie vždy je to tak.
Môže vám slúžiť: hodnotné riešeniaAj keď v batériách je anóda pozitívnym stĺpom, v LED svetlách je to opak, anóda je záporným pólom.
Normálne je definovaný zmysel pre elektrický prúd, ktorý ho oceňuje ako zmysel pre voľné zaťaženie, ale ak vodič nie je kovový, kladné náboje sa prenesú na externý vodič.
Tento pohyb znamená, že máme pozitívne a negatívne náboje, ktoré sa pohybujú v opačných zmysloch, takže sa hovorí, že smer prúdu je cesta kladných nábojov katiónov, ktoré sú v anóde smerom k negatívnemu zaťaženiu anód anód Anódy, ktoré sa nachádzajú v katóde.
V galvanických bunkách, ktorý má kovový vodič, prúd generovaný v reakcii sleduje cestu od pozitívneho pólu k negatívnemu.
Ale v elektrolytických bunkách, ktoré nemajú kovový vodič, ale elektrolyt, ióny s pozitívnym a negatívnym zaťažením, ktoré sa pohybujú v opačných zmysloch.
Termoionické anódy dostávajú väčšinu elektrónov, ktoré pochádzajú z katódy, zohriali anódu a musia nájsť spôsob, ako rozptýliť. Toto teplo sa vytvára v napätí, ktoré sa vyskytuje medzi elektrónmi.
Špeciálne anódy
Existuje typ špeciálnych anód, ako sú napríklad v rámci X -Rays. V týchto skúmavkách vytvára energia produkovaná elektrónmi okrem výroby X -Rays.
Toto teplo sa vyskytuje s rôznym napätím medzi oboma elektródami a ktoré vyvíja tlak na elektróny. Keď sa elektróny pohybujú v elektrickom prúde, zasiahli anódu vysielaním tepla.
Môže vám slúžiť: Henderson-Haselbalchova rovnica: Vysvetlenie, príklady, cvičenieKatóda
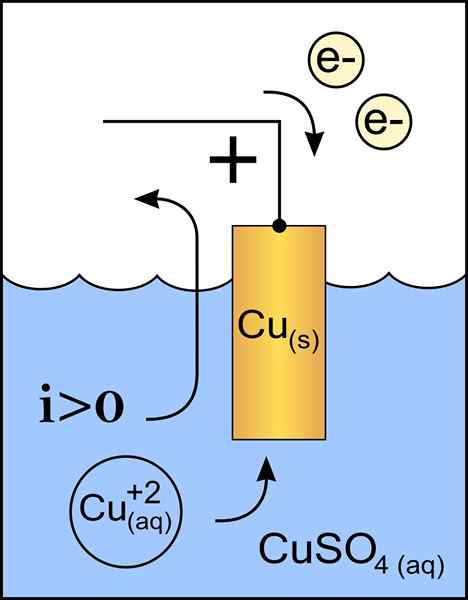 Diagram medi v voltaickej bunke. Zdroj: Originálna práca: Súbor: Zinková anóda 2.PNG od používateľa: Micheljullian (talk) Derivát Work: KES47/CC BY-S (http: // creativecommons.Org/licencie/By-SA/3.0/)
Diagram medi v voltaickej bunke. Zdroj: Originálna práca: Súbor: Zinková anóda 2.PNG od používateľa: Micheljullian (talk) Derivát Work: KES47/CC BY-S (http: // creativecommons.Org/licencie/By-SA/3.0/) Katóda je elektróda s negatívnym zaťažením, ktorá v chemickej reakcii trpí redukčnou reakciou, kde je jej oxidačný stav znížený, keď prijíma elektróny.
Rovnako ako v prípade anódy, aj Faraday, ktorý navrhol termín katód, ktorý pochádza z gréckeho κατά [catá]: „dole“ a ὁδός [Odós]: „Road“. K tejto elektróde sa v priebehu času pripisovalo záporné zaťaženie.
Tento prístup bol nepravdivý, pretože v závislosti od zariadenia, v ktorom sa nachádza, má zaťaženie alebo iný.
Tento vzťah s negatívnym pólom, rovnako ako pri anóde, vyplýva z predpokladu, že prúd tečie z pozitívneho pólu na negatívny. To vzniká vo vnútri galvanickej bunky.
V elektrolytických bunkách môžu prostriedky prenosu energie, pretože nie sú v kovovom, ale v elektrolyte, môžu koexistovať negatívne a pozitívne ióny, ktoré sa pohybujú v opačných zmysloch. Ale na základe dohody sa hovorí, že prúd ide z anódy do katódy.
Špeciálne katódy
Typ špecifických katódov sú termionické katódy. V týchto katódach emituje elektróny v dôsledku účinku tepla.
V termionických ventiloch sa katóda môže zahrievať cirkuláciou vykurovacieho prúdu vo vlákne, ktorý ho má spojený.
Rovnovážna reakcia
Ak vezmeme galvanickú bunku, ktorá je najbežnejšou elektrochemickou bunkou, môžeme formulovať rovnovážnu reakciu, ktorá sa generuje.
Každá semi -stredi, ktorá tvorí galvanickú bunku, má charakteristické napätie známe ako redukčný potenciál. V každom semi -stredii existuje oxidačná reakcia medzi rôznymi iónmi.
Môže vám slúžiť: absorpčné spektrumKeď táto reakcia dosiahne rovnováhu, bunka nemôže poskytnúť väčšie napätie. V tejto dobe bude mať oxidácia, ktorá sa odohráva v semi -stredi tohto okamihu. Potenciál reakcie bude väčší, tým väčšia rovnováha sa dosiahne.
Keď je anóda v rovnováhe, začne strácať elektróny, ktoré prechádzajú vodičom do katódy.
V katóde dochádza k redukčnej reakcii, čím ďalej bude mať najnáročnejšia rovnováha reakciu pri výrobe a užívaní elektrónov, ktoré pochádzajú z anódy.
Odkazy
- Huheey, James a., a kol.Anorganická chémia: Princípy štruktúry a reaktivity. Pearson Education India, 2006.
- Sienko, Michell J.; Robert, a.Chémia: princípy a vlastnosti. New York, USA: McGraw-Hill, 1966.
- Brady, James a.Všeobecná chémia: princípy a štruktúra. Wiley, 1990.
- Petrucci, Ralph H., a kol.Všeobecná chémia. Inter -American Educational Fund, 1977.
- Masterton, William L.; Hurley, Cecile n.Chémia: princípy a reakcie. Cengage Learning, 2015.
- Charlot, Gaston; Tremillon, Bernard; Badoz-Lambling, J. Elektrochemické reakcie. Toray-Masson, 1969.
- « 10 najdôležitejších príspevkov a vynálezov
- Quetzálne charakteristiky, biotop, reprodukcia, jedlo »

