Vlastnosti, štruktúra, použitia, riziká, riziká oxalátu vápenatého (CAC2O4)
- 4285
- 833
- MUDr. Žigmund Boška
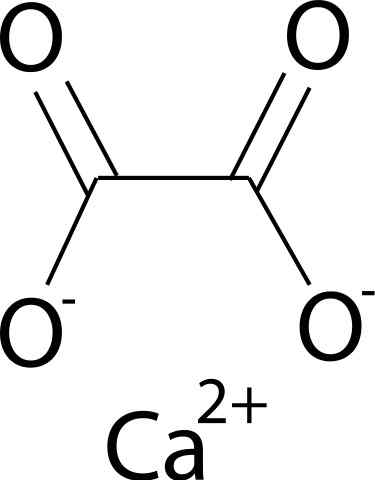
On Oxalát vápenatého Je to organická zlúčenina tvorená prvkami uhlíka (C), kyslíka (O) a vápniku (CA) (CA) (CA). Jeho chemický vzorec je CAC2Ani4. Všeobecne sa nachádza vo svojich troch hydratovaných formách: mono-, di- a trihydrát. Toto je s jedným, dvoma alebo tromi molekulami vody vo svojej kryštalickej štruktúre.
Oxalát vápenatého sa nachádza v mineráloch, rastlinách, húb a iných živých bytostiach, ako sú cicavce a dokonca aj u ľudí v dôsledku metabolizmu niektorých proteínov. Nachádza sa v moči ľudí a niektorých zvierat.
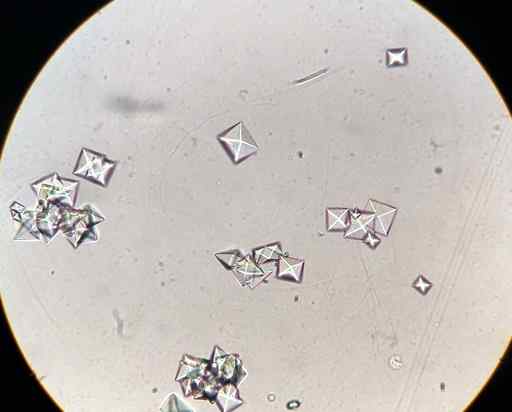 Kryštály oxalátu vápenatého CAC2Ani4 Vo vzorke moču pozorovanej mikroskopom. J3D3/CC BY-SA (https: // creativeCommons.Org/licencie/By-SA/4.0). Zdroj: Wikimedia Commons.
Kryštály oxalátu vápenatého CAC2Ani4 Vo vzorke moču pozorovanej mikroskopom. J3D3/CC BY-SA (https: // creativeCommons.Org/licencie/By-SA/4.0). Zdroj: Wikimedia Commons. Niektoré potraviny ako špenát, Ruibarbos, sój.
Môžete sa vyhnúť vzhľadu kameňov CAC2Ani4 V obličkách, ak sa požíva veľa tekutín, najmä voda, vyhýbajúc sa potravinám s vysokým obsahom oxalátu a konzumáciou tých bohatých na vápnik a horčík.
Oxalát vápenatého tvorí nežiaduce vložky do potrubí a procesných nádrží, ako je výroba buničiny a papiera a tiež v továrňach na pivné továrne.
[TOC]
Štruktúra
Oxalát vápenatého je tvorený iónom vápenatého2+ a oxalátový ión C2Ani42-. Oxalátový anión pozostáva z dvoch atómov uhlíka a štyroch atómov kyslíka. Negatívne zaťaženie oxalátového aniónu sa nachádza v atómoch kyslíka.
 Chemická štruktúra oxalátu vápenatého. Vsimonian/CC By-SA (https: // creativeCommons.Org/licencie/By-SA/2.5). Zdroj: Wikimedia Commons.
Chemická štruktúra oxalátu vápenatého. Vsimonian/CC By-SA (https: // creativeCommons.Org/licencie/By-SA/2.5). Zdroj: Wikimedia Commons. Menovanie
- Oxalát vápenatého
- Vápniková soľ kyseliny oxalovej
- Kyselina s kyselinou etanodioovej vápniková soľ
Vlastnosti
Fyzický stav
Bezfarebná kryštalická, biela, žltá alebo hnedá, ktorá môže byť v troch rôznych hydratovaných formách.
Molekulová hmotnosť
128,1 g/mol
Bod topenia
Monohydráty oxalátu vápenatého sa rozkladá na 200 ° C.
Špecifická váha
Monohydrát CAC2Ani4 •H2O = 2,22 g/cm3
Dihydrát CAC2Ani4 •2h2O = 1,94 g/cm3
Trihydrát CAC2Ani4 •3h2O = 1,87 g/cm3
Rozpustnosť
Takmer nerozpustné vo vode: 0,00061 g/100 g vody pri 20 ° C. Monohydrát sa rozpúšťa v zriedenej kyseline.
pH
Vodné roztoky oxalátu vápenatého sú slabo základné.
Chemické vlastnosti
Oxalát vápenatého je vápniková soľ kyseliny oxalovej. Je to prírodný sekundárny produkt metabolizmu, takže je veľmi hojný v ľudskom tele a je súčasťou mnohých potravín.
Kyselina oxalová a jej konjugovaná báza, oxalát, sú veľmi oxidované organické zlúčeniny s silnou chelatačnou aktivitou, to znamená, že sa dajú ľahko kombinovať s pozitívnymi iónmi s +2 alebo +3 zaťaženiami.
Môže vám slúžiť: metyl alebo metilo skupinaJeho vodné roztoky sú slabo základné, pretože oxalátový ión má tendenciu brať protóny h+ vody, ktorá uvoľňuje Oh ióny-. Po vzatí dvoch protónov h+ Oxalátový ión sa stáva kyselinou oxalovou h2C2Ani4:
C2Ani42- + H2O → HC2Ani4- + Oh-
HC2Ani4- + H2O → h2C2Ani4 + Oh-
Prítomnosť v prírode
V mineráloch
Oxalát vápenatého je najbežnejším oxalátom a je prezentovaný vo forme minerálov nazývaných whewellita, weddellita a caoxit.
Whewellita je CAC monohydrát2Ani4 •H2Alebo je najstabilnejšia z foriem tejto zlúčeniny.
 Whewellita Mineral Rock. Rob Lavinsky, Irocks.com-ccy-SA-3.0/cc By-SA (https: // creativeCommons.Org/licencie/By-SA/3.0). Zdroj: Wikimedia Commons.
Whewellita Mineral Rock. Rob Lavinsky, Irocks.com-ccy-SA-3.0/cc By-SA (https: // creativeCommons.Org/licencie/By-SA/3.0). Zdroj: Wikimedia Commons. Weddellita je dihydrát CAC2Ani4 •2h2O a je menej stabilný ako monohydrát.
 Weddelite minerálne kryštály. Leon Hupperichs/CC od (https: // creativeCommons.Org/licencie/o/3.0). Zdroj: Wikimedia Commons.
Weddelite minerálne kryštály. Leon Hupperichs/CC od (https: // creativeCommons.Org/licencie/o/3.0). Zdroj: Wikimedia Commons. Caxita je CAC oxalátu vápenatého Trihydrado CAC2Ani4 •3h2Ani.
V rastlinách a húb
Oxalát vápenatého je spojený so suchými pôdami a listami, tiež s patogénmi, voľnými, symbiózami alebo rastlinami spojenými s rastlinami. V poslednom uvedenom prípade sú kryštály tvorené zrážaním vápnika vo forme jeho oxalátu.
Tvorba CAC2Ani4 V prípade húb má dôležitý vplyv na biologické a geochemické procesy pôdy, pretože predstavuje rezervu vápnika pre ekosystém.
Prítomnosť v ľudskom tele a u cicavcov
Oxalát pochádza z pečene, v krvných bunkách červených alebo erytrocytov av menšom množstve v obličkách. Vytvára sa z metabolizmu aminokyselín (ako je fenylalanín a tryptofán) a oxidáciou glioxálneho dialdehydu,.
Vitamín C sa môže tiež stať oxalátom pri vykonávaní svojej antioxidačnej funkcie.
Oxalát vápenatého sa nachádza v kameňoch, ktoré sa tvoria v obličkách ľudí alebo zvierat s ochorením obličiek.
Výpočty alebo kamene s oxalátom vápenatého oxalátu sa tvoria kryštalizáciou alebo agregáciou CAC2Ani4 V celkovom moči s vápnikom a oxalátom. To znamená, že moč obsahuje vápnik aj oxalát, že nie je možné, že zlúčenina zostáva rozpustená, ale vyzráža alebo prechádza do tuhého stavu vo forme kryštálov.
U ľudí
Tvorba piesku alebo kameňov v obličkách je choroba nazývaná nefrolitiáza; Útočí na približne 10% populácie a asi 75% týchto kameňov je zložených z CAC oxalátu vápenatého oxalátu2Ani4.
 Oxalát vápenatého môže tvoriť kamene v obličkách. Autor: VSRAO. Zdroj: Pixabay.
Oxalát vápenatého môže tvoriť kamene v obličkách. Autor: VSRAO. Zdroj: Pixabay. Tvorba a rast kryštálov oxalátu vápenatého v obličkách sa vyskytuje, pretože u niektorých ľudí je moč presýtený uvedenou soľou. Oxalát vápenatého sa vyvíja v kyslom moči pri pH menej ako 6,0.
Môže vám slúžiť: IsóbarosSufeatraturácia dochádza, keď sa vylučovanie alebo eliminácia tejto soli (ktorá je veľmi málo rozpustná vo vode) cez moč v malom objeme vody.
Faktory, ktoré ovplyvňujú vzhľad obličkových kameňov
Medzi faktormi, ktoré uprednostňujú tvorbu piesočnatého oxalátu vápenatého, patrí nadmerný vápnik v moči alebo hyperkalciúrii, nadbytok oxalátu v moči alebo hyperoxalúrii, prvky odvodené z kŕmenia a neprítomnosť inhibítorov.
Prebytočný oxalát sa môže vyskytnúť, keď sa požívajú veľké množstvo špenátu, drsné, sójové orechy a čokoláda,.
 Čokoláda môže byť zdrojom oxalátu vápenatého a uprednostňuje vzhľad kameňov v obličkách. Autor: Alexander Stein. Zdroj: Pixabay.
Čokoláda môže byť zdrojom oxalátu vápenatého a uprednostňuje vzhľad kameňov v obličkách. Autor: Alexander Stein. Zdroj: Pixabay. Existujú však látky, ktoré inhibujú alebo bránia tvorbe kameňov. Medzi zlúčeniny, ktoré sa vyhýbajú výpočtom, sú malé molekuly, ako je citrát a pyrofosfát, a veľké molekuly, ako sú glykoproteíny a proteoglykány.
Spôsoby, ako sa vyhnúť tvorbe kameňov oxalátu vápenatého
Dobrá stratégia na zabránenie výpočtu recidívy piesku alebo výpočtu oxalátu vápenatého vrátane zvýšenia požitia tekutín, zvýšenia potravín rozbitých vápnika (ako napríklad mliečne výrobky) a obmedzenia stolovej soli (NACL), živočíšnych bielkovín, živočíšnych bielkovín a bohatých jedál v oxalácii v oxalácii.
U zvierat
Od začiatku roka 2000. Zdá sa, že to závisí od typu potravín, ktoré tieto zvieratá požívajú a súvisia s kyslosťou nedostatku moču a horčíka (MG).
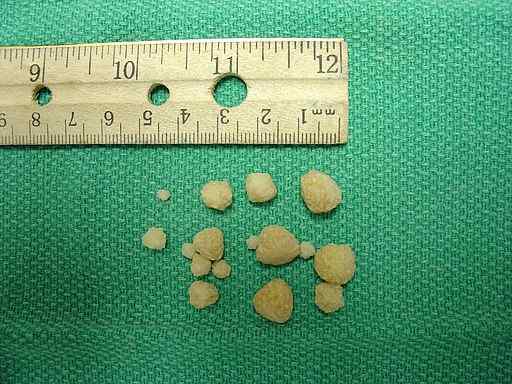 Kamene oxalátu vápenatého nachádzajúce sa v močovom mechúre psa. Joel Mills/CC BY-SA (http: // creativeCommons.Org/licencie/By-SA/3.0/). Zdroj: Wikimedia Commons.
Kamene oxalátu vápenatého nachádzajúce sa v močovom mechúre psa. Joel Mills/CC BY-SA (http: // creativeCommons.Org/licencie/By-SA/3.0/). Zdroj: Wikimedia Commons. Reakcia tela na nadmerný oxalát
Existujú dôkazy o tom, že ľudia aj zvieratá reagujú na nadmerný oxalát zvýšením počtu baktérií, ktoré môžu degradovať oxalát.
Niektoré z týchto baktérií sú Oxalobacter formigény, Bifidobacterium sp., Porphyromonas gingivalis a Bacillus SP., okrem iného a sú prirodzene prítomné v čreve.
Žiadosti
Podľa konzultovaných zdrojov sa oxalát vápenatý používa v keramickom povlaku.
Používa sa na pokrytie sochy a iných umeleckých prvkov vápenca a zistilo sa, že zlepšuje tvrdosť materiálu, znižuje jeho pórovitosť a zvyšuje jeho odolnosť voči kyselinám a alkalis.
 V Taliansku sa týkalo pokrývania predmetov vápencový múzeá s oxalátom vápenatého na ich zachovanie. Autor: Zdroj: Moni Quayle. Pixabay.
V Taliansku sa týkalo pokrývania predmetov vápencový múzeá s oxalátom vápenatého na ich zachovanie. Autor: Zdroj: Moni Quayle. Pixabay. Problémy v niektorých procesoch
V priemysle buničiny a papiera môže oxalát vápnika tvoriť vložky, ktoré v procese spôsobujú veľa problémov.
Aby sa predišlo jeho tvorbe v priemyselných procesoch alebo potrubiach.
Môže vám slúžiť: chlorid kobaltu (COCL2 (: štruktúra, nomenklatúra, vlastnostiMá tiež tendenciu hromadiť sa ako kameň v nádobách, kde sa vyrába pivo.
Riziká
Vo vysokých koncentráciách môže oxalát spôsobiť smrť u zvierat a občas u ľudí kvôli jeho korozívnym účinkom hlavne kvôli jeho korozívnym účinkom.
Hromadenie oxalátu a jeho konjugovanej kyseliny, kyseliny oxalovej, môže spôsobiť poruchy, ako je porucha srdca, kamene oxalátu vápenatého, zlyhanie obličiek a dokonca smrť z toxicity.
Odkazy
- Glasauer, s.M. a kol. (2013). Kovy a metaloidy, transformácia mikroorganizmami. Oxaláty. V referenčnej modulácii v zemských systémoch a environmentálnych vedách. Zotavené z vedeckých pracovníkov.com.
- Baumann, J. M. a Casella, r. (2019). Prevencia vápenatej nefrolitiázy: Vplyv diurézy na kryštalizáciu oxalátu vápenatého v moči. Adv Previum, 2019; 2019: 3234867. NCBI sa zotavila.NLM.NIH.Vláda.
- Breshears, m.Do. a udeliť,.W. (2017). Močový systém. Vápenaté výpočty. V patologickom základe veterinárnych chorôb (šieste vydanie). Zotavené z vedeckých pracovníkov.com.
- Huang a. er al. (2019). Manipulácia s oxalátom v telesnom telese TGE a pôvodu oxalátu v kameni oxalátu vápenatého oxalátu. Urol Int, 2019 5. decembra: 1-10. NCBI sa zotavila.NLM.NIH.Vláda.
- Nilvebrant, n.-Ani. a kol. (2002). Biotechnológia v priemysle buničiny a papiera. Prebieha v biotechnológii. Zotavené z vedeckých pracovníkov.com.
- Pahira, J.J. A Pevzner, m. (2007). Nefrolitiáza. Vápnikové kamene. V Penn Clinical Manual of Urology. Zotavené z vedeckých pracovníkov.com.
- Worcester, e. M. (1994). Inhibítory rastu kryštálov oxalátu moču. J Am Soc Nephrol 1994 Nov; 5 (5 Suppl 1): S46-53). Zotavený z Jasn.Asnjournál.orgán.
- Finkielstein, V.Do. a Goldfarb, D.Siež. (2006). Stratégie na prevenciu kameňov oxalátu vápenatého. NCBI sa zotavila.NLM.NIH.Vláda.
- Alebo.Siež. Lekárska knižnica. (2019). Oxalát vápenatého. Obnovený z pubchem.Ncbi.NLM.NIH.Vláda.
- Peck, a.B. a kol. (2015). Mikroorganizmy degratujúce oxalát alebo enzýmy degratujúce oxalát: WICH je budúcou terapiou enzymatického rozpustenia urolitov oxalátu vápnika-oxalátu pri opakujúcich sa ochoreniach kameňa? Urolitiasis, 2016 február; 44 (1): 27-32. NCBI sa zotavila.NLM.NIH.Vláda.
- Holames, r.P. a kol. (2016). Zníženie vylučovania oxalátu moču na dekréciu Diepar oxalátu vápenatého oxalátu. Urolitiáza. 2016 február; 44 (1); 27-32. NCBI sa zotavila.NLM.NIH.Vláda.
- Cyzar, T.M. (1998). Oxalát vápenatého: povrchové ošetrenie vápenca. Journal of Conservation and Museum Studies 4, s.6-10. Zdroj z JCMS-Journal.com.
- Wikimedia (2019). Oxalát vápenatého. Získaný z.Wikipedia.orgán.
- « Kvalitatívne výskumné charakteristiky, typy, techniky, príklady
- Funkcionalizmus (psychológia) pôvod, charakteristiky a zástupcovia autorov »

