Henryho zákon

- 2451
- 145
- Ing. Ervín Petruška
 Henryho zákon vysvetľuje šumenie nealkoholických nápojov
Henryho zákon vysvetľuje šumenie nealkoholických nápojov Aký je Henryho zákon?
Ten Henryho zákon Je to vzťah, ktorý opisuje vplyv tlaku na rozpustnosť plynu. Tento zákon uvádza, že rozpustnosť plynu v kontakte s povrchom kvapaliny pri danej teplote je priamo úmerná čiastočnému tlaku uvedeného plynu na kvapalinu.
To znamená, že čím väčší tlak plynu na kvapalinu, tým väčšie je celkové množstvo plynu, ktoré sa v ňom môže rozpustiť, a tým získanie väčšej koncentrácie (to znamená, tým väčšia je rozpustnosť).
Henryho zákon Vidíme to v akcii zakaždým, keď odhalíme sódu nápoj. Vysoký tlak vo vnútri fľaše udržiava rozpustený uhľovodíkový plyn. Ale jeho odhalením sa znižuje tlak plynu, čo znižuje jeho rozpustnosť a unikne tvoriacich bubliny a šumenie.
Henryho zákona o zákone
V matematickej podobe je Henryho zákon vyjadrený ako zákon o proporcionalite:
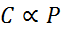
Tento zákon o proporcionalite sa zmení na:
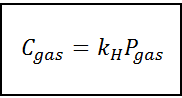
Kde C Vzťahuje sa na maximálnu koncentráciu plynu v kvapaline, to znamená jeho rozpustnosť; Pplyn Je to čiastočný tlak plynu v kontakte s kvapalinou a klimatizovaťH Je to proporcionálna konštanta nazývaná Henryho zákona.
Koncentrácia plynu môže byť vyjadrená v rôznych jednotkách, ako je molarita, moleita alebo molárna frakcia. Vo väčšine prípadov však chemikálie používajú koncentráciu v molaritných jednotkách (v mol/l), zatiaľ čo tlak je vyjadrený v atmosfére.
Môže vám slúžiť: Antracén: Čo je, štruktúra, vlastnosti, použitieKonštanta Henryho zákona (klimatizovaťH)
Konštanta klimatizovaťH Opíšte interakcie medzi plynom a rozpúšťadlom. Čím silnejšie sú tieto interakcie, tým väčšia je konštanta, a tým väčšia je rozpustnosť plynu v rozpúšťadle pri určitej teplote a tlaku.
Numericky, hodnota klimatizovaťH predstavuje rozpustnosť plynu pri danej teplote, keď je čiastočný tlak z 1 atm.
V závislosti od jednotiek koncentrácie a tlaku použitého v rovnici môže táto konštanta mať mol/l jednotky.bankomat, mol/kg.bankomat atď.
Nasledujúca tabuľka ukazuje hodnoty konštanty Henryho zákona pre niektoré bežné plyny vo vode pri 25 ° C:

Tieto hodnoty klesajú s teplotou, pretože rozpustnosť plynov všeobecne klesá pri vyššej teplote.
Vysvetlenie Henryho zákona
Henryho zákon je z mikroskopického hľadiska veľmi ľahko pochopiteľný. Dokážeme si predstaviť plyn ako sadu veľmi malých častíc odrážajúcich na všetkých povrchoch, ktoré hrajú. Keď sa zrazia s povrchom kvapaliny, niektoré častice sa odrazia, zatiaľ čo iné prechádzajú cez uväznené povrchy (to znamená, že sa rozpustia).
To isté platí pre rozpustené častice plynu. Odrazia sa so stenami nádoby a môžu tiež dosiahnuť povrch kvapaliny, kde sa niektorí odrazia, zatiaľ čo iní prechádzajú povrchom a uniknú do plynovej fázy.
Keď sa dosiahne rovnováha, rýchlosti, s akou sa plyn rozpustí v rozpúšťadle a s ktorým uniká, sú rovnaké, takže koncentrácia zostáva konštantná.
Môže vám slúžiť: Mechanické vlastnosti kovov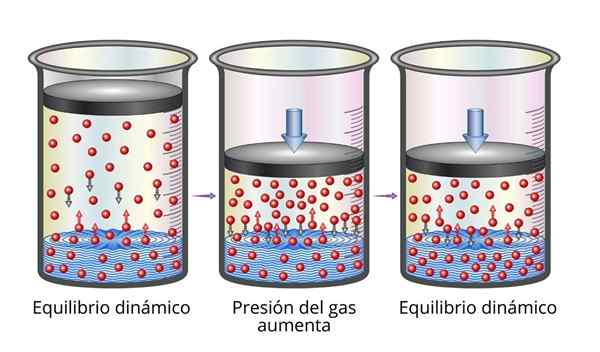 Vysvetlenie Henryho zákona
Vysvetlenie Henryho zákona Keď zvyšujeme tlak plynu, robíme to, že zvýšite frekvenciu, s akou sa častice plynu zrážajú s povrchom kvapaliny. Vďaka tomu sa rýchlosť, s akou sa plyn rozpúšťa, sa zvyšuje. Ak sa dosiahne nová rovnováha, bude nová koncentrácia plynu vyššia.
Výnimky z Henryho zákona
Je dôležité zdôrazniť, že Henryho zákon je ideálny zákon, ktorý opisuje iba správanie skutočných riešení plynu za určitých podmienok. Henryho zákon sa teda dá uplatniť iba vtedy, keď:
- Teplota zostáva konštantná.
- Plyn je v rovnováhe s roztokom.
- Tlak plynu je relatívne nízky.
- Plyn nereaguje s rozpúšťadlom.
Napriek tomu, aj v niektorých prípadoch, keď plyn reaguje s rozpúšťadlom, je možné tento zákon uplatniť približne.
Príklady uplatňovania Henryho zákona
Príklad 1: Určenie konštanty Henryho zákona
Experimentálne sa zistilo, že koncentrácia vodného roztoku v rovnováhe s neónom pri tlaku 3,00 atm a 25 ° C je 0,00135 mol/l. Stanovte konštantu Henryho zákona pre neón vo vode pri 25 ° C.
Riešenie:
Podľa Henryho zákona:
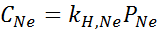
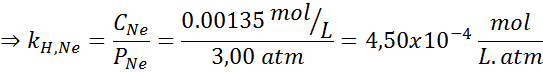
Preto je Henryho zákona o konštante pre neónov vo vode pri 25 ° C 4,50 × 10-4 mol/l.Bankomat.
Príklad 2: Stanovenie rozpustnosti plynu
Pomocou konštanty Henryho zákona poskytnutého v predchádzajúcej tabuľke určte rozpustnosť oxidu uhličitého vzduchu vo vode na hladine mora, pretože viem, že molárna frakcia uvedeného plynu vo vzduchu je 3,14 × 10-4.
Riešenie:
Na hladine mora je tlak vzduchu 1 atm a čiastočný tlak CO2 Je daný:
Môže vám slúžiť: kyselina hypoyodózna (HIO)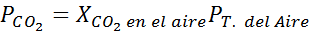
Nahradenie tohto výrazu v Henryho zákone:
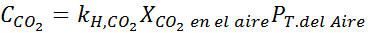
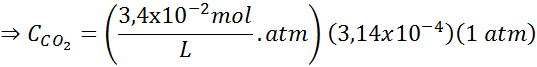
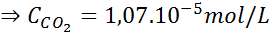
Príklad 3: potápačské plyny
Keď potápač nič v hĺbke viac ako 30 metrov, zmes vzduchu musí dýchať s inými inertnými plynmi, ako je hélium alebo argón, pretože zvýšenie koncentrácie dusíka v predpovedanej krvi podľa Henryho zákona má narkotické účinky, ktoré spôsobujú dezorientáciu, zmätenie a videnie. problémy.
Tento efekt začína pozorovať pri dýchaní vzduchu (xN2= 0,78) pri tlaku 4,00 atm. Ak potápač plánuje zostúpiť hlboko až 100 metrov, kde je tlak okolo 11,0 bankom?
Riešenie:
Na základe vyhlásenia dokážeme vyvodiť, že maximálna koncentrácia dusíka je to, čo sa vyskytuje, keď je tlak vzduchu 4,00 ATM. Podľa Henryho zákona a používania vzťahu medzi celkovým tlakom a čiastočným tlakom predchádzajúceho príkladu:
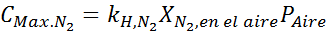
To musí byť rovnaká maximálna koncentrácia pri akomkoľvek celkovom tlaku. Takže 100 metrov:
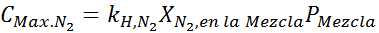
Vyrovnanie oboch rovníc môžeme nájsť maximálnu molárnu frakciu dusíka v zmesi:
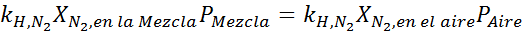
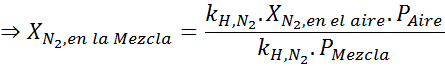
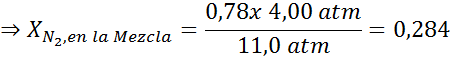
To znamená, že potápač by nemal používať zmes obsahujúcu viac ako 28,4% dusíka, ak plánuje ponoriť sa až do 100 metrov hlboký.

