Chemické javy charakteristiky a príklady

- 3569
- 1038
- Alan Milota
Ten Chemické javy Sú to všetci tí, ktorí chápu sériu chemických reakcií, ktoré sú prezentované v každodennom živote. Aj keď je pravda, že chemické reakcie je možné študovať alebo vykonávať v laboratóriu, chemické javy je možné vidieť kdekoľvek; vonku v oblakoch, v našich organizmoch alebo v tej istej kuchyni.
Niektoré príklady chemických zmien sú spaľovanie dreva, strávenie jedla, varenie vajíčka, oxidácia železa, pečenie koláča, hniloba ovocia, pečenie mäsa, výbuch ohňostrojov, okrem iného.
 Pečenie sušienok je jedným z nespočetných denných chemických javov, ktoré všetci pozná. Zdroj: HolMespj cez Pixabay.
Pečenie sušienok je jedným z nespočetných denných chemických javov, ktoré všetci pozná. Zdroj: HolMespj cez Pixabay. Je ľahké rozpoznať chemické javy, hoci nie sú izolované, ale spolu s fyzikálnymi (alebo biologickými) zmenami. Hovorí sa, že k chemickému javu došlo, keď došlo k zvýšeniu teploty, uvoľňovania plynu, náhleho osvetlenia, tvorby zrážania; alebo zmeny vône, farby alebo textúry.
Všetky chemické javy však spoločne zdieľajú transformáciu na identitu hmoty; Rozbitie odkazov na vytvorenie nových, zmiznutie činidiel na generovanie výrobkov.
„Jednoduchý“ chemický jav môže zahŕňať alebo vypláchnuť veľké množstvo chemických reakcií, ktoré sa riadia jedným alebo viacerými mechanizmami. K tomu dochádza, najmä keď varíme, pečieme.
[TOC]
Charakteristika
Každá samostatná chemická reakcia má súbor charakteristík, ktorá im umožňuje byť rozpoznávanie alebo klasifikácia od ostatných; Nech sú tieto dvojité vytesnenie (metatéza), zrážky, neutralizácia, pridanie, izomerizácia, redukcia oxidu, hydrogenácia, spaľovanie, pyrolýza, zubonifikácia, polymerizácia a mnoho ďalších.
Niektoré z nich môžu byť reverzibilné (výrobky tvoria činidlá) alebo nezvratné (existujú iba tvorba produktu). Podobne sú niektoré exotermické, endotermické, pomalé alebo rýchle (s alebo bez katalyzátora).
Môže vám slúžiť: Disposio: Štruktúra, vlastnosti, získanie, použitieVšetci sa však zhodujú na zmene identity hmoty (atóm, funkčná skupina, molekula atď.). To spôsobuje variáciu v jednej z vlastností systému, ktoré sa stávajú: farba, zápach, teplota, tlak, viskozita, hmotnosť, objem, hustota, index lomu,.
Je tiež bežné pozorovať bublajúce, vzhľad zrazeniny alebo dvojitých fáz, zábleskov alebo výbuchov. Chemický jav sa potom charakterizuje zobrazením kombinácie takýchto zmien a môže tiež pozostávať zo série reakcií alebo transformácií úzko spojených so sebou navzájom.
Preto, v závislosti od hranolu, s ktorým sa vizualizuje, chemické javy predovšetkým narážajú na všetky prírodné alebo každodenné procesy, v ktorých sa považuje za jednu alebo viac súčasných chemických reakcií.
Príklady
Minerálna kryštalizácia
 Niektoré minerály kryštalizujú odparovaním vody. Zdroj: pxhere.
Niektoré minerály kryštalizujú odparovaním vody. Zdroj: pxhere. Aj keď nie všetky mechanizmy minerálnej kryštalizácie sú striktne chemické javy, keď pochádzajú z vodného roztoku, ktorý sa pomaly odparuje, zatiaľ čo ióny sú zoskupené a tvoria slané kryštály.
Vodné prúdy môžu pretiahnuť ióny hornín do iných oblastí, kde sa konečne odparia a zanechajú stopu kryštálov; Ako sa to napríklad stane, v Los Lagos de Sales.
Spaľovanie

Kde je oheň, je energická a vysoko exotermická oxidácia. Pri osvetlení hlavy zápasu horí s kyslíkom vzduchu, čím sa vytvorí oxidy, čo nielen vyplýva tepla, ale aj kvôli zmene farby v červenej na čierne zhody.
Oheň je preto chemický jav, ktorý znamená tvorbu mnohých oxidov; Aj keď sa vyskytne v lese, džungli alebo horách, budú sa skladať takmer z oxidu uhoľnatého, ako aj z oxidov dusíka a síry.
Môže vám slúžiť: Hypertonické riešenieKyslý dážď

Kyslý dážď je chemický jav, ktorý zahŕňa hydratáciu niekoľkých oxidov plynnej kyseliny (nieX, SW3, Clo2, Co2). Tieto plynné oxidy, keď sa interagujú s vodnými kvapkami mrakov3, H2SW4, HCLO3, H2Co3), ktoré sa nakoniec vypúšťajú v daždi.
Kyslé dažde sa vyznačujú svojím vysokým obsahom HNO3 a h2SW4, Ovplyvňujú vodné ekosystémy, sejby, okysliteľné voda a zhoršujú mramorové sochy.
Výroba a zhoršenie ozónu
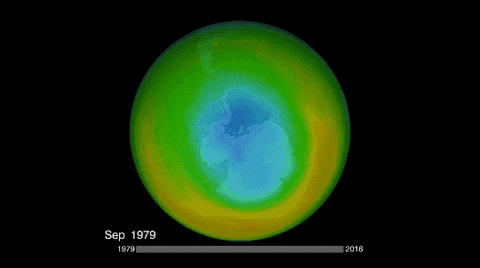
Stratosférický ozón sa vyskytuje, keď kyslík reaguje s ultrafialovým žiarením slnka; a jeho prirodzená deštrukcia, hoci rôznym mechanizmom, znova regeneruje kyslík.
Existujú však chemické druhy, ktoré sa z dôvodu ultrafialového žiarenia rozkladajú vo voľných radikáloch, ktoré ničia ozón, čo ho inhibujú jeho ochranné pôsobenie.
Fermentácia
Fermentácia je príkladom chemického javu, pretože mikroorganizmy katalyzujú reakcie na organický substrát, ktorým je zvyčajne jedlo, šťava alebo pitie, aby sa vytvorila drastická zmena jeho organoleptických vlastností; najmä podľa jeho chuti, ako je to v prípade piva a vína.
Variť
 Varenie je vykonať sériu chemických javov, takže z ingrediencií sa vyrábajú raňajky, obed alebo večera. Zdroj: Milly Eaton cez pexels.
Varenie je vykonať sériu chemických javov, takže z ingrediencií sa vyrábajú raňajky, obed alebo večera. Zdroj: Milly Eaton cez pexels. Kniha bola napísaná vo všetkých chemických javoch, ktoré sa konajú, keď varíme. Na začiatok, použitie ohňa už znamená denaturáciu proteínov, ktoré integrujú jedlo, ich dehydratáciu a rozklad určitých odkazov na generovanie výrobkov, ktoré zintenzívňujú ich príchute a farby.
Varte vajce, pečte chlieb alebo sušienky, smažte kuracie mäso alebo steaky, pripravte si kávu, tepelné cestoviny, šalát šalátu s octom, fermentové ananásy, pridajte citrón do ryby, aby ste neutralizovali prchavé amíny atď., Sú to príklady v podstate chemických javov.
Karamelizácia a reakcia Maillard
 Pri príprave syrového karamelu sa používa karamelizačná reakcia cukru. Zdroj: Guillermo Amador (Flickr.com)
Pri príprave syrového karamelu sa používa karamelizačná reakcia cukru. Zdroj: Guillermo Amador (Flickr.com) Ďalším konkrétnym chemickým javom, ktorý sa často vyskytuje v kuchyni, je karamelizácia. Skladá sa z čiastočného spaľovania sladkého roztoku, kým sa nezmení zlatý alebo hnedý; To znamená, že sa zastaví práve v čase, keď je karamel pripravený.
Môže vám slúžiť: cykloalcinosCukry sa začínajú dehydratovať tepelným pôsobením, aby vznikli kompendium molekúl; Niektoré malé (Furanona a Maltol), vďaka ktorej má cukríky svoju charakteristickú vôňu; Iné polymérne (karamelín a cukríky), zodpovedné za farby karamelu.
Keď sú cukry sprevádzané okrem proteínu.
Opäť je typické pozorovať chemický jav, ktorý zahŕňa takúto reakciu pri pečení cookies alebo obilnín biscu atď.
Bioluminiscencia
 Osvetlené pobrežie pláže v noci vďaka bioluminiscencii dinoflagelovaných rias. Zdroj: Jed zo San Diega v Kalifornskej republike [CC BY-SA 2.0 (https: // creativeCommons.Org/licencie/By-SA/2.0)]
Osvetlené pobrežie pláže v noci vďaka bioluminiscencii dinoflagelovaných rias. Zdroj: Jed zo San Diega v Kalifornskej republike [CC BY-SA 2.0 (https: // creativeCommons.Org/licencie/By-SA/2.0)] Nakoniec, a v neposlednom rade alebo zvedaví, máme bioluminiscenciu, kde organizmy alebo bytosti sú schopné generovať pôsobením luciferázového enzýmu na luciferínové proteín, jeho vlastné svetlo. Jasný príklad je možné vidieť v svetlometoch a ich žltá bliká cez noc.
Odkazy
- Whitten, Davis, Peck & Stanley. (2008). Chémia. (8. vydanie.). Učenie sa.
- Triasť a Atkins. (2008). Anorganická chémia. (Štvrté vydanie). MC Graw Hill.
- Elsevier. (2019). Chemické javy. Zdroj: ScienceDirect.com
- HelMestine, Anne Marie, PH.D. (16. októbra 2019). Príklad chemických reakcií v každodennom živote. Zotavené z: Thoughtco.com
- Wikipedia. (2019). Chemická reakcia. Zdroj: In.Wikipedia.orgán
- Univerzita. (2019). Klasifikácia chemických reakcií. Zdroj: Openstax.orgán
- Biomimicry Institute. (27. januára 2017). Chémia prírody. Získané z: Asknature.orgán
- Ashley Hamer. (14. mája 2018). 10 spôsobov, ako hacknúť varenie s chémiou. Získané z: zvedavosti.com
- Úrok. (2018). Potravinová chémia - Maillardova reakcia. Získané z: zlúčeniny.com
- Ashish. (25. marca 2018). Prečo cukor pri roztopení zhnedne? Získané z: ScienceABC.com
- « Charakteristiky Lactofenolovej modrej, zloženie, príprava, použitia
- Štruktúra hydroxidu vápenatého (Ca (OH) 2), vlastnosti, získanie, použitie, použitia »

