Tepla absorbované vzorce, ako ich vypočítať a vyriešiť cvičenia

- 987
- 71
- MUDr. Žigmund Boška
On absorbované teplo Je definovaný ako prenos energie medzi dvoma telami pri rôznych teplotách. Ten s nižšou teplotou absorbuje teplo, ako je pri vyššej teplote. Keď sa to stane, zvyšuje sa tepelná energia látky, ktorá absorbuje teplo, a častice, ktoré ho tvoria rýchlejšie, zvyšujú svoju kinetickú energiu.
To sa môže premietnuť do zvýšenia teploty alebo zmeny stavu. Napríklad prejdite z tuhej k tekutine, ako je napríklad ľad, keď sa topí v kontakte s vodou alebo sódou pri izbovej teplote.
 Kovová čajová lyžička absorbuje horúcu kávu. Zdroj: Pixabay.
Kovová čajová lyžička absorbuje horúcu kávu. Zdroj: Pixabay. Vďaka teplu je tiež možné, že objekty menia svoje rozmery. Tepelná dilatácia je dobrým príkladom tohto javu. Keď sa zohrieva väčšina látok, zvyčajne zažívajú zvýšenie svojich rozmerov.
Výnimkou z toho je voda. Rovnaké množstvo kvapalnej vody zvyšuje svoj objem, keď sa ochladí pod 4 ° C. Okrem toho môžu zmeny teploty zažiť aj zmeny na úrovni ich hustoty, niečo tiež veľmi pozorovateľné v prípade vody.
[TOC]
Čo je a vzorce
V prípade energie pri tranzite sú jednotkami absorbovaného tepla jouly. Avšak na dlhú dobu malo teplo svoje vlastné jednotky: kalórie.
Dnes sa táto jednotka používa na kvantifikáciu energetického obsahu potravín, aj keď v skutočnosti potravinová kalória zodpovedá kilokalitu tepla.
Kalórie
Kalórie, skrátene ako vápno, Je to množstvo tepla potrebného na zvýšenie teploty 1 gramu vody o 1 ° C.
V devätnástom storočí Sir James Prescott Joule (1818 - 1889) uskutočnil slávny experiment, v ktorom sa mu podarilo transformovať mechanickú prácu na teplo, čím získal nasledujúcu rovnocennosť:
1 kalórie = 4.186 joules
V britských jednotkách sa tepelná jednotka nazýva BTU (Britská tepelná jednotka), ktorý je definovaný ako množstvo tepla potrebného na zvýšenie teploty libry vody za 1 ° F.
Môže vám slúžiť: Kalibračná krivka: Na čo je to, ako to urobiť, príkladyRovnocennosť medzi jednotkami je nasledovná:
1 Btu = 252 kalórií
Problém s týmito starými jednotkami je v tom, že množstvo tepla závisí od teploty. To znamená, že nie je to isté, čo sa vyžaduje na prechádzanie z 70 ° C na 75 ° C, ako napríklad voda potrebná na zahriatie vody z 9 ° C na 10 ° C,.
Preto definícia uvažuje o dobre definovaných intervaloch: 14.5 až 15.5 ° C a 63 až 64 ° F pre kalórie a BTU.
Čo závisí od množstva absorbovaného tepla?
Množstvo absorbovaného tepla, ktoré zhromažďuje materiál, závisí od niekoľkých faktorov:
- Masa. Čím vyššia je hmotnosť, tým viac tepla je schopná absorbovať.
- Charakteristika látok. Existujú látky, ktoré sú v závislosti od ich molekulárnej alebo atómovej štruktúry schopné absorbovať viac tepla ako iné.
- Teplota. Je potrebné pridať viac tepla, aby sa získala vyššia teplota.
Množstvo tepla, označované ako Otázka, Je úmerný opísaným faktorom. Preto môžete písať ako:
Q = m.c.ΔTón
Kde m Je to hmotnosť objektu, c je konštanta nazývaná špecifické teplo, vnútorná vlastnosť látky a δTón Je to teplotná variácia dosiahnutá absorbovaním tepla.
Δt = tF - Tónani
Tento rozdiel má pozitívny znak, pretože pri absorbovaní tepla sa dá očakávať TónF > Tani. Stáva sa to, pokiaľ látka zažíva fázovú zmenu, napríklad vodu, keď prechádza parná tekutina. Keď voda vrie, jej teplota zostáva konštantná pri približne 100 ° C, bez ohľadu na to, ako rýchlo sa varí.
Ako ho vypočítať?
Kontaktovaním dvoch objektov pri inej teplote, po chvíli dosahujú tepelnú rovnováhu. Teploty sa teda vyrovnávajú a prenos tepla prestane. To isté sa stane, ak je v kontakte viac ako dva objekty. Po určitom čase budú mať všetci pri rovnakej teplote.
Môže vám slúžiť: magnetizácia: orbitálny a rotátny magnetický moment, príkladyZa predpokladu, že objekty v kontakte tvoria uzavretý systém, z ktorého sa teplo nemôže uniknúť, uplatňuje sa princíp ochrany energie, takže je možné potvrdiť, že:
Otázka pohltený = - Q Zasadiaci
To predstavuje energetickú bilanciu, podobnú výdavku na vchody a výdavky osoby. Z tohto dôvodu má ceded teplo záporné znamenie, pretože pre objekt, ktorý sa poskytuje, je konečná teplota nižšia ako počiatočná. Preto:
Δt = tF - Tónani < 0
Rovnica q pohltený = - Q Zasadiaci Používa sa vždy, keď sú v kontakte dva objekty.
Energetická bilancia
Na vykonanie energetickej bilancie je potrebné rozlíšiť objekty, ktoré absorbujú teplo, ktoré poskytujú, potom:
Σ qklimatizovať= 0
To znamená, že súčet ziskov a straty energie v uzavretom systéme sa musí rovnať 0.
Špecifické teplo látky
Na výpočet množstva absorbovaného tepla musíte poznať špecifické teplo každej zúčastnenej látky. Toto je množstvo tepla potrebného na zvýšenie teploty 1 g materiálu o 1 ° C. Jej jednotky v medzinárodnom systéme sú: Joule/kg . Klimatizovať.
Existujú tabuľky so špecifickým teplom mnohých látok, ktoré sa všeobecne vypočítavajú pomocou kalorimetra alebo podobných nástrojov.
Príklad toho, ako vypočítať špecifické teplo materiálu
Na zvýšenie teploty kovového krúžku 20 až 30 ° C sa vyžaduje 250 kalórií. Ak má prsteň hmotnosť 90 g. Aké je špecifické teplo tepla v jednotkách SI?
Riešenie
Jednotky sa najprv prevedú:
Q = 250 kalórií = 1046.5 J
m = 90 g = 90 x 10-3 kg
Môže vám slúžiť: elastické otrasy: v rozmere, špeciálne prípady, cvičenia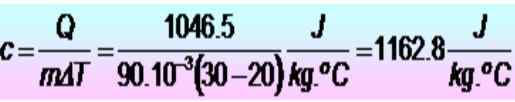
Cvičenie
Hliníková šálka obsahuje 225 g vody a 40 g medeného miešania, všetko pri 27 ° C. Vzorka 400 g striebra pri počiatočnej teplote 87 ° C sa vloží do vody.
Miešadlá sa používa na miešanie zmesi, až kým nedosiahne svoju konečnú rovnovážnu teplotu 32 ° C. Vypočítajte hmotnosť hliníkového pohára, vzhľadom na to, že voči životnému prostrediu nedochádza k tepelným stratám.
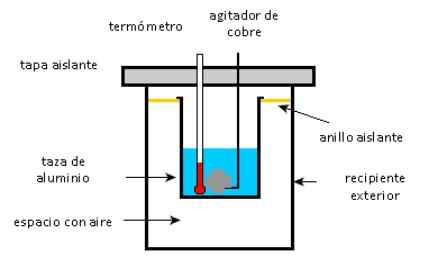 Schéma kalorimetra. Zdroj: SolidSwiki.
Schéma kalorimetra. Zdroj: SolidSwiki. Prístup
Ako je uvedené vyššie, je dôležité rozlíšiť objekty, ktoré poskytujú teplo od tých, ktoré absorbujú:
- Hliníkový šálka, meď a voda a voda Absorbujú teplo.
- Vzorka striebra poskytuje teplo.
Údaje
Dodáva sa špecifické teploty každej látky:
- Striebro: C = 234 J/kg. ° C
- Meď: C = 387 j/kg. ° C
- Hliník C = 900 J/kg. ° C
- Voda C = 4186 J/kg. ° C
Teplo absorbované alebo priradené každou látkou sa vypočíta rovnicou:
Q = m.c.λTón
Riešenie
Striebro
Otázka Zasadiaci = 400 x 10 -3 . 234 x (32 - 87) j = -5148 j
Meď
Otázka pohltený = 40 x 10 -3 . 387 x (32 - 27) J = 77.4 J
Vodná voda
Otázka pohltený = 225 x 10 -3 . 4186 x (32 - 27) J = 4709.25 J
Hliníkový pohár
Otázka pohltený = m hliník . 900 x (32 - 27) J = 4500 .m hliník
Využívanie:
Σ qklimatizovať= 0
77.4 + 4709.25 + 4500 .m hliník = - (-5148)
Nakoniec je hliníková hmota vyčistená:
m hliník = 0.0803 kg = 80.3 g
Odkazy
- Giancoli, D. 2006. Fyzika: Princípy s aplikáciami. 6th. Edimatizovať. Sála. 400 - 410.
- Kirkpatrick, L. 2007. Fyzika: pohľad na svet. 6ubytovať sa Skrátene vydanie. Učenie sa. 156 - 164.
- Rex, a. 2011. Základy fyziky. Pearson. 309 - 332.
- Sears, Zemansky. 2016. Fyzika univerzity s modernou fyzikou. 14th. Objem1. 556 - 553.
- Serway, r., Vulle, C. 2011. Základy fyziky. 9nat Učenie sa. 362 - 374

